| 物竞编号 | 0817 |
|---|---|
| 分子式 | CH3Li |
| 分子量 | 21.97 |
| 标签 | 甲基锂标准品, Lithium methanide, MeLi, Methyllithium solution, 金属有机物 |
编号系统
CAS号:917-54-4
MDL号:MFCD00008253
EINECS号:213-026-4
RTECS号:暂无
BRN号:3587162
PubChem号:24885367
物性数据
1. 性状:未确定
2. 密度(g/mL,20/4℃):0.85 g/mL
3. 相对蒸汽密度(g/mL,空气=1):3
4. 熔点(ºC):未确定
5. 沸点(ºC,常压):35℃
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:未确定
8. 闪点(ºF):5 °F
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:不溶于烃类溶剂;能适当溶于醚类溶剂;与水和其它质子性溶剂反应生成甲烷。
毒理学数据
生态学数据
对水是稍微有害的,不要让未稀释或大量的产品接触地下水,水道或者污水系统,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:2
8.表面电荷:0
9.复杂度:2
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:2
性质与稳定性
1.常温常压下稳定,避免氧化物 酸 水分接触。
2.非溶剂化的固体易自燃;在没有LiBr的情况下,乙醚中的甲基锂容易自燃;而其它常见的配方(无论液体或者固体)都不会自燃。
贮存方法
密封保存在低温、干燥并且有惰性气体保护的容器中。
合成方法
在一个装有磁力搅拌器,气体导入管和干冰冷凝管的1刃的三颈瓶中,放入800毫升无水乙醚和托克(2.3克原子)锉丝,在连续搅拌下4一5小时内向反应瓶内蒸入100克(1.05摩尔)嗅甲烷,然后将此混合物搅拌1小时。在氮气流中放置过夜以使不溶物沉淀,在氮气中将上层清液转移到干燥的有橡皮盖的贮液管或容器中

用途
1.用途碱性试剂和还原剂。用于丙二烯合成。a一轻酮转变成顺式二醇,从梭酸制酮。分解醋酸醋。使烯醇乙酸醋成烯醇负离子制a一溴代酮或a,一不饱和酮。合成螺戊烷。从丫一酮酸醋制日一二酮。与日、丫一不饱和酸反应成醋a芳香醛酮的甲基化一还.原。烯基砜的锉化。
2.甲基锂可以对多种官能团进行甲基化,可以脱除保护基团,合成其它甲基化有机金属试剂,可以作为碱以及还原过渡金属等。溶剂和卤素对用到非溶剂化的甲基锂的反应有很大的影响。
加成反应 与甲基格氏试剂相比,甲基锂与环烃、杂环以及脂肪族化合物的1,2-加成反应有不同的选择性。与酮的亲核加成由于螯合反应而有高的非对映选择性 (式1)[1]。另外,这个反应的立体选择性也受其它一些Lewis酸的影响。

把有机锂转化为有机钛、有机铈或者有机锌后会提高其立体选择性。例如,将甲基锂转化为手性钛与苯甲醛发生1,2-加成,产物ee值达到99% (式2)[2]。

用酸和酯作用经常会得到甲基酮,而用三甲基氯硅烷处理这个反应将会得到更好的结果。对于用烷氧羰基和苯甲酰基保护的二级酰肼来说,甲基锂是一个很好的脱酰基试剂。将甲基锂与溴化锂共同与甲硅烷基酮在0 oC作用,会高立体选择性地得到甲硅烷基烯醇醚 (式3)[3]。

腈、亚胺以及唑烷都可以作为碳氮不饱和键的1,2-加成的底物。例如,在异丙基苯/THF中,甲基锂与保护的氰醇加成,水解后得到很高产率的甲基甾族酮[7]。而四嗪、吡嗪等芳香杂环的加成反应就很难进行。芳香亚胺可以在具有C2 对称性的三级二胺的催化下,与甲基锂发生对映选择性的加成 (式4)[4]。

其它反应 甲基锂可以与邻烯丙基苯甲酰胺成环生成萘酚衍生物 (式5)[5]。
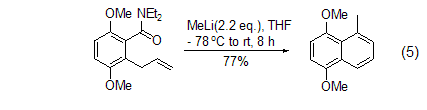
甲基锂使环丙基衍生物的偕二溴化物发生重排得到丙二烯衍生物和一溴取代物的混合物。甲基锂还可以与偕二溴代环丁烷作用,脱除溴重排得到亚烷基环丙烷 (式6)[6]。
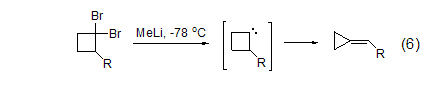
安全信息
危险运输编码:UN 3399 4.3/PG 1
危险品标志: 易燃
易燃  腐蚀
腐蚀  危害环境
危害环境
安全标识:S16 S26 S43 S45 S60 S36/S37/S39
文献
1. Maruoka, K.; Itoh, T.; Sakurai, M.; Nonoshita. K.; Yamamoto, H. J. Am. Chem. Soc., 1988, 110, 3588. 2. (a) Reetz, M. T.; Kyung, S. H.; Huellman, M. Tetrahedron, 1986, 42, 2931. (b) Reetz, M. T.; Hugel, H.; Dresely, K. Tetrahedron, 1987, 43, 109. 3. Reich, H. J.; Holtan, R. C.; Bolm, C. J. Am. Chem. Soc., 1990, 112, 5609. 4. (a) Kizirian, J. C.; Caille, J. C.; Alexakis, A. Tetrahedron Lett., 2003, 44, 8893. (b) Kizirian, J. C.; Cabello, N.; Pinchard, L.; Caille, J. C.; Alexakis, A. Tetrahedron, 2005, 61, 8939. 5. Sibi, M. P.; Dankwardt, J. W.; Snieckus, V. J. Org. Chem., 1986, 51, 271. 6. Nordvik, T.; Mieusset, J. L.; Brinker, U. H. Org. Lett., 2004, 6, 715. 7.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无







 沪公网安备 31010602001115号
沪公网安备 31010602001115号