| 物竞编号 | 095Q |
|---|---|
| 分子式 | P2O5 |
| 分子量 | 141.94 |
| 标签 | 无水磷酸, 磷酸酐, 五氧化磷, Phosphorus pentoxide, Phosphorous oxide (P2O5), Phosphoric anhydride, Diphosphorus pentoxide, 脱水干燥剂, 有机合成缩合剂, 表面活性剂 |
编号系统
CAS号:1314-56-3
MDL号:MFCD00011440
EINECS号:215-236-1
RTECS号:TH3945000
BRN号:暂无
PubChem号:24867015
物性数据
1.性状:白色粉末,不纯品为黄色粉末,易吸潮。[11]
2.熔点(℃):340~360[12]
3.沸点(℃):360(升华)[13]
4.相对密度(水=1):2.39[14]
5.相对蒸气密度(空气=1):4.9[15]
6.饱和蒸气压(kPa):0.13(384℃)[16]
7.溶解性:不溶于丙酮、氨水,溶于硫酸。[17]
毒理学数据
1.急性毒性[18] LC50:1217mg/m3(大鼠吸入,1h)
2.刺激性 暂无资料
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
4.其他有害作用[19] 该物质对环境有危害,应特别注意对水体的污染。
分子结构数据
1、摩尔折射率:无可用的
2、摩尔体积(cm3/mol):无可用的
3、等张比容(90.2K):无可用的
4、表面张力(dyne/cm):无可用的
5、介电常数:无可用的
6、极化率(10-24cm3):无可用的
7、单一同位素质量:141.922095 Da
8、标称质量:142 Da
9、平均质量:141.9445 Da
计算化学数据
1、 疏水参数计算参考值(XlogP):-2.4
2、 氢键供体数量:0
3、 氢键受体数量:10
4、 可旋转化学键数量:0
5、 互变异构体数量:
6、 拓扑分子极性表面积(TPSA):124
7、 重原子数量:14
8、 表面电荷:0
9、 复杂度:327
10、 同位素原子数量:0
11、 确定原子立构中心数量:0
12、 不确定原子立构中心数量:0
13、 确定化学键立构中心数量:0
14、 不确定化学键立构中心数量:0
15、 共价键单元数量:1
性质与稳定性
1.溶于水生成磷酸。固体物氧化磷有三种晶形。H型:属于亚稳定性,熔点为420℃,沸点为340℃,升华温度为360℃。O型:斜方晶形,H型在封闭管中400℃加热2h则变为O型,熔点为562℃,沸点为605℃。O′(T)型:正方晶系,H型在封闭管中于450℃加热24h则生成O’(T)型,熔点为580℃,沸点为605℃。
2.稳定性[20] 稳定
3.禁配物[21] 钾、钠、水、醇类、碱类、过氧化物
4.避免接触的条件[22] 潮湿空气
5.聚合危害[23] 不聚合
6.分解产物[24] 氧化磷
贮存方法
储存注意事项[25] 储存于阴凉、干燥、通风良好的库房。远离火种、热源。库温不超过25℃,相对湿度不超过75%。包装必须密封,切勿受潮。应与活性金属粉末、碱类、过氧化物、醇类等分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
1.氧化法 将黄磷加热熔融后,送入氧化燃烧炉,用干燥空气(经浓硫酸脱水)进行氧化燃烧反应,生成五氧化二磷因受热而升华,在炉顶遇冷而落入氧化燃烧炉底部的沉降室内,制得五氧化二磷成品。由氧化燃烧炉逸出的尾气经旋风分离器以回收五氧化二磷粉尘。回收成品与沉降室中的产品一起作为成品包装。其4P+5O2→2P2O5以试剂级五氧化二磷为原料,在充分干燥的氧气气流中灼烧升华提纯,经冷凝器捕集升华物,制得高纯五氧化二磷成品。
2.在广口瓶上安装一个用马口铁制成的宽口漏斗,漏斗上倒罩着一个比漏斗口小的衬锡的马口铁圆筒(直径350mm,高500mm)。圆筒底部装入通气弯管,中上部开有一口,是用来安装燃烧勺用的。加热燃烧勺,向勺中放入干燥的白磷,迅速插入圆筒中,并借燃烧勺柄上的塞子固定在圆筒上。当磷烧尽后再重复此操作。通气强度和燃烧速度可由调节圆筒与漏斗间的缝隙大小控制。燃烧生成的氧化磷在圆筒内壁上冷却。轻轻敲动圆筒就落入广口瓶中。提纯市场上或上述所制得的氧化磷常含有磷的低价氧化物,有时还含有黄磷,一般实验可直接使用,欲需要较纯的可进一步在干燥的氧气流中灼烧升华制取。将一干燥清洁的T型管倒置,管口上安装放有起始原料的P2O5玻管。从T型管的一端通入经CaCl2干燥的氧气,另一端接玻璃冷却管。将待灼烧升华的P2O5放入T型管中加热。200g市售样品在2h后可得到大约70g纯品。以试剂级五氧化二磷为原料,在充分干燥的氧气气流中灼烧升华提纯,经冷凝器捕集升华物,制得高纯五氧化二磷成品。
3.在预先经浓硫酸、固体氢氧化钾和工业品五氧化二磷干燥过的纯氧气流作用下,将工业品五氧化二磷升华提纯,可得不含低级氧化物的五氧化二磷。
用途
1.用作生产高纯度磷酸、磷酸盐类和磷酸酯的原料,也用于五氧化二磷溶胶和以H型为主的气溶胶的制造。
2.可用作气体和液体的干燥剂、有机合的脱水剂。合成纤维的抗静电剂及糖的精制剂。还用于制造光学玻璃、透紫外线玻璃、隔热玻璃、微晶玻璃和乳浊玻璃等,以提高玻璃的色散系数和透过紫外线的能力。
3.五氧化二磷主要用于干燥剂、有机合成的脱水剂和关环反应的催化试剂。
酰胺脱水成腈 酰胺用五氧化二磷脱水可以制备腈。未取代的酰胺与过量的五氧化二磷共蒸馏可以高产率制备腈 (式1)[1]。很多反应是在无溶剂条件下进行的,有时可以用高沸点的溶剂。

催化重排反应 10%浓度的五氧化二磷甲磺酸溶液 (Eaton试剂) 是有效的酸性环合试剂,可以有效的代替多磷酸 (PPA),例如用于Beckman重排 (式2,式3)[2,3]。

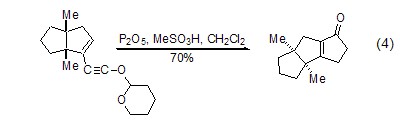
Eaton试剂还能促进共轭不饱和炔类化合物关环 (式4)[4]。
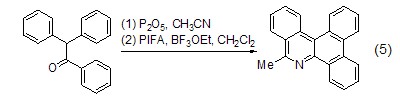
脱水环合反应 P2O5在高温下能使反应物脱水而环化 (式5)[5],这是制备异喹啉的一个重要方法。
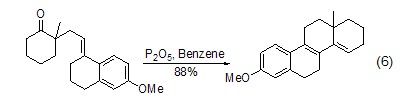
合成脂环化合物时,P2O5也是非常有效的关环的催化剂 (式6)[6]。
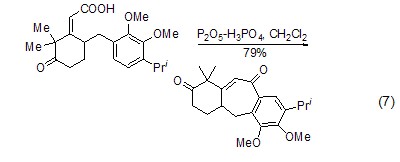
有时要加入磷酸促进关环的进行 (式7)[7]。
合成含氮杂环 通过加热五氧化二磷和含氮酮或醇是一种合成含氮杂环化合物的通用方法 (式8,式9)[8,9]。
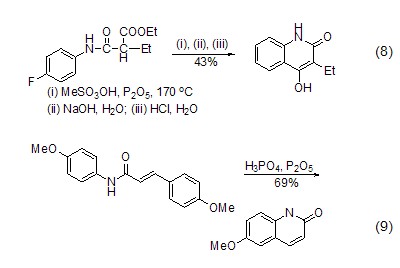
合成碘代物 在磷酸/五氧化二磷的催化下,一级醇与KI反应得到1-碘代物 (式10)[10]。
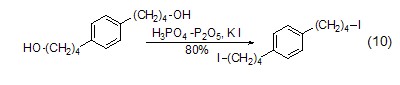
4.用作干燥剂、脱水剂,用于制造高纯度磷酸、磷酸盐及农药等。[26]
安全信息
危险运输编码:UN 1807 8/PG 2
危险品标志: 腐蚀
腐蚀
危险标识:R35
文献
1. Camps, P.; Munoz-Torrero, D.; Simon, M. Synth. Commun., 2001, 31, 3507. 2. Hilmey, G. D.; Paquette, L. A. Org. Lett., 2005, 7, 2067. 3. Eshghi, H.; Gordi, Z. Synth. Commun., 2003, 33, 2971. 4. Srikrishna, A.; Dethe, D. H. Org. Lett., 2003, 5, 2295. 5. Churruca, F.; SanMartin, R.; Carril, M.; Urtiaga, M. K.; Solans, X.; Tellitu, I.; Dominguez, E. J. Org. Chem., 2005, 70, 3178. 6. Saraber, F. C. E.; Groot, A. Tetrahedron Lett., 2004, 45, 9431. 7. Ning, C.; Wang, X.; Pan, X. Synth. Commun., 1999, 29, 2115. 8. Freeman, G. A.; Andrews, C. W. III; Hopkins, A. L.; Lowell, G. S.; Schaller, L.T.; Cowan, J. R.; Gonzales, S. S.; Koszalka, G. W.; Hazen, R. J.; Boone, L. R.; Ferris, R. G.; Creech, K. L.; Roberts, G. B.; Short, S. A.; Weaver, K.; Reynolds, D. J.; Milton, J.; Ren, J.; Stuart, D. I.; Stammers, D. K.; Chan, J. H. J. Med. Chem., 2004, 47, 5923. 9. Inglis, S. R.; Stojkoski, C.; Branson, K. M.; Cawthray, J. F.; Fritz, D.; Wiadrowski, E.; Pyke, S. M.; Booker, G. W. J. Med. Chem., 2004, 47, 5405. 10. Hamze, A.; Rubi, E.; Arnal, P.; Boisbrun, M.; Carcel, C.; Salom-Roig, X.; Maynadier, M.; Wein, S.; Vial, H.; Calas, M. J. Med. Chem., 2005, 48, 3639. [1~10]参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7 [11~26]参考书:危险beplay体育首页 安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号