| 物竞编号 | 08BR |
|---|---|
| 分子式 | C12H27P |
| 分子量 | 202.32 |
| 标签 | TBP |
编号系统
CAS号:998-40-3
MDL号:MFCD00009462
EINECS号:213-651-2
RTECS号:SZ3270000
BRN号:1738261
PubChem号:暂无
物性数据
1. 性状:未确定
2. 密度(g/ mL,25℃):0.81
3. 相对蒸汽密度(g/mL,空气=1):9
4. 熔点(ºC):-65
5. 沸点(ºC,常压):未确定
6. 沸点(ºC,50mmHg):150
7. 折射率(n
8. 闪点(ºF):99
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶解于大多数有机溶剂,微溶于乙腈和水。可以用31P NMR检测试剂纯度。
毒理学数据
1、急性毒性:大鼠口经LD50:750mg/kg
生态学数据
通常对水是不危害的,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):3.7
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:9
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:13
8.表面电荷:0
9.复杂度:72.1
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.易燃且有臭味。
2.若储存不当,可能产生三丁基氧膦和二丁基亚膦酸丁酯。因此使用前通常需要经过减压蒸馏进行纯化。
贮存方法
可以在室温下保存,需要惰性气体保护,必须严格除氧,以免自由基链反应而被氧化。
合成方法
暂无
用途
与大多数常用的三配位磷试剂不同,三丁基膦是一种亲核试剂。它是相对较弱的碱(在MeNO3中pKa = 8.70;在甲醇中pKa = 5.60),使用时溶剂不必严格除氧,但需要用惰性气体保护,若暴露在空气中会发生剧烈的氧化反应,生成三丁基氧膦和二丁基亚膦酸丁酯。
硫醚与硫酯的合成 三丁基膦与二硫化物及醇反应可生成相应的硫醚和Bu3PO;与二硫化物和羧基反应可以得到硫酯 (式1)[1]。
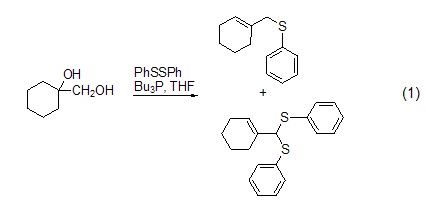
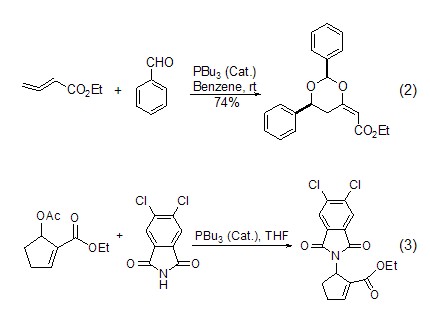
催化羰基与烯烃的加成反应 由于三丁基膦具有亲核性,进攻双键后会导致电子云的偏移,从而发生加成反应。如通过苯甲醛与丙二烯的成环反应 (式2)[2]。
催化亲核取代反应 三丁基膦还可用作亲核取代反应的催化剂,如它可以催化邻苯二甲酰胺与烷氧基的取代反应 (式3)[3]。
催化1,4-加成反应 三丁基膦也是最常用的1,4-加成反应的催化剂。因为三丁基膦具有亲核性和弱碱性,它比其它三配位磷催化剂 (如三苯基膦等) 更适于催化此类反应。因此三丁基膦是合成环反应 (式4)[4] 的重要催化剂之一。
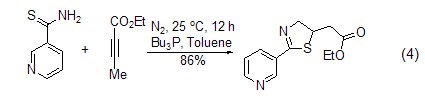
催化C-X键的生成 三丁基膦还可以活化叠氮化合物,从而形成碳-氮双键。这类反应常用于关环等合成路线 (式5)[5]。另外三丁基膦还可用于叠氮膦的烷基化反应 (式6)[6]。
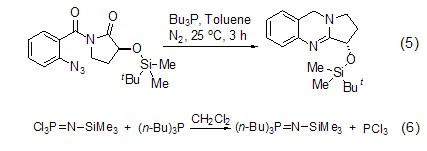
C-C键的形成 三丁基膦可以催化不饱和烃与芳香化合物的偶联反应 (式7)[7],以及α-位有离去基团的烯烃的偶联反应。其中后者常被用作关环反应 (式8)[8]。

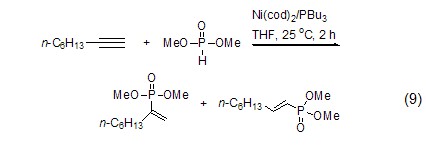
作为金属催化剂的配体 三丁基膦可以与一些金属催化剂共同使用,从而催化不同类型的反应,如与Ni共同催化亚磷酸酯的烷基化反应 (式9)[9]。
安全信息
危险运输编码:UN 3254 4.2/PG 1
危险品标志: 易燃
易燃  腐蚀
腐蚀
安全标识:S17 S26 S43 S45 S36/S37/S39
文献
1. Shinada, T.; Yoshida, Y.; Ohfune, Y. Tetrahedron Lett., 1998, 39, 6027. 2. Zhu, X.-F.; Henry, C. E.; Wang, J.; Dudding, T.; Kwon, O. Org. Lett., 2005, 7, 1387. 3. Cho, C.-W.; Kong, J.-R.; Krische, M. J. Org. Lett., 2004, 6, 1337. 4. Liu, B.; Davis, R.; Joshi, B.; Reynolds, D. W. J. Org. Chem., 2002, 67, 4595. 5. Eguchi, S.; Suzuki, T.; Okawa, T.; Matsushita, Y.; Yashima, E.; Okamoto, Y. J. Org. Chem., 1996, 61, 7316. 6. Rivard, E.; Huynh, K.; Lough, A. J.; Manners, I. J. Am. Chem. Soc., 2004, 126, 2286. 7. Koech, P. K.; Krische, M. J. J. Am. Chem. Soc., 2004, 126, 5350. 8. Krafft, M. E.; Haxell, T. F. N. J. Am. Chem. Soc., 2005, 127, 10168. 9. Han, L.-B.; Zhang, C.; Yazawa, H.; Shimada, S. J. Am. Chem. Soc., 2004, 126, 5080. 10.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无









 沪公网安备 31010602001115号
沪公网安备 31010602001115号