| 物竞编号 | 07P1 |
|---|---|
| 分子式 | C18H16Si |
| 分子量 | 260.41 |
| 标签 | 三苯基硅烷, 三苯硅烷, TPS, 硅烷试剂 |
编号系统
CAS号:789-25-3
MDL号:MFCD00003003
EINECS号:212-333-0
RTECS号:暂无
BRN号:978182
PubChem号:24848907
物性数据
1. 性状:无色晶体
2. 密度(g/mL,25/4℃):未确定
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):43-45
5. 沸点(ºC,常压):未确定
6. 沸点(ºC, 2 mm Hg):152
7. 折射率:未确定
8. 闪点(ºF):169
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶解于大多数有机溶剂,许多反应在CH2Cl2或者THF中进行。
毒理学数据
暂无
生态学数据
对水是稍微有害的,不要让未稀释或大量的产品接触地下水,水道或者污水系统,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:3
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:19
8.表面电荷:0
9.复杂度:202
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
该试剂在常温、常压和空气中稳定。由于反应需要在自由基引发剂或者强酸的存在下进行,建议在通风橱中进行操作。
贮存方法
储存在干爽的惰性气体下,保持容器密封,储存在阴凉,干燥的地方。
合成方法
由三苯基氯硅烷用氢化锂或四氢锂铝还原制取。
用途
1.用来合成有机硅中间体。
2.三苯基硅烷 (TPS) 在有机合成中被定义为具有特殊功能的还原剂和氢硅化试剂。TPS所还原的对象主要是羰基、羟基和羟基羧酸酯,大多数通常的还原剂不具备这些功能。
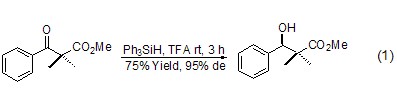
TPS 的特殊功能之一是在三氟乙酸存在下方便地除去叔醇中的羟基生成相应的烃[1]。但是,酮羰基在该条件下能够被还原成相应的仲醇。由于TPS本身和反应体系价格较贵,该反应主要应用于酮羰基的立体选择性还原反应。此时,TPS立体位阻较大的结构特点便可以得到体现 (式1)[2]。
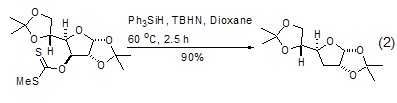
TPS的另一种特殊功能是在自由基引发剂二叔丁基过氧化物 (DTPB) 的存在下,将羧酸酯还原成烃。不同的羧酸酯类型中以乙酸酯最容易被还原,但是反应仍然需要在高温下进行[3,4]。如果使用硫代酯的话,反应条件可以温和许多,而且产率也有所提高 (式2)[5,6]。这可能是由于硫化物对该反应有催化作用。
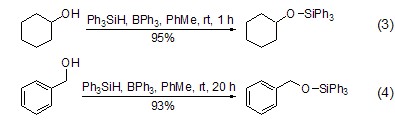
TPS也常常用于醇和酚的硅醚化反应,许多不同类型的催化剂均可以催化O-Si键的生成 (式3,式4)[7,8]。
炔烃的氢硅化反应是TPS参与的重要反应。反应主要受到过渡金属或者路易斯酸的催化[9~12]。硅烷的类型和体积对反应的产率和产物中顺反异构体的选择性影响不是太大,而催化剂的类型和性质才是关键的影响因素。例如:1-己炔在钌催化作用下主要生成顺式产物 (式5),而使用铂催化剂几乎全部生成反式产物 (式6)。

安全信息
危险运输编码:暂无
危险品标志: 刺激
刺激
安全标识:S26
危险标识:R36/37/38
文献
1. Carey, F. A.; Tremper, H. S. J. Org. Chem., 1971, 36, 758. 2. Hamashima, Y.; Yagi, K.; Takano, H.; Tamas, L.; Sodeoka, M. J. Am. Chem. Soc., 2002, 124, 14530. 3. Sano, H.; Ogata, M.; Migita, T. Chem. Lett., 1986, 77. 4. Ishiwata, A.; Ito, Y. Synlett, 2003, 9, 1339. 5. Dang, H. S.; Roberts, B. P.; Tocher, D. A. J. Chem. Soc., Perkin Trans. 1, 2001, 2452. 6. Cai, Y.; Roberts, B. P. Tetrahedron Lett., 2001, 42, 763. 7. Le Bideau, F.; Henique, J.; Samuel, E.; Coradin, T. Chem. Commun., 2001, 1408. 8. Blackwell, J. M.; Foster, K. L.; Beck, V. H.; Piers, W. E. J. Org. Chem., 1999, 64, 4887. 9. Sudo, T.; Asao, N.; Gevorgyan, V.; Yamamoto, Y. J. Org. Chem., 1999, 64, 2494. 10. Commandeur, C.; Thorimbert, S.; Malacria, M. J. Org. Chem., 2003, 68, 5588. 11. Na, Y.; Chang, S. Org. Lett., 2000, 2, 1887. 12. Aneetha, H.; Wu, W.; Verkade, J. G. Organometallics, 2005, 24, 2590. 13.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无








 沪公网安备 31010602001115号
沪公网安备 31010602001115号