| 物竞编号 | 07VT |
|---|---|
| 分子式 | C4H9KO |
| 分子量 | 112.21 |
| 标签 | Potassium t-butoxide, Potassium tert-butylate, 强碱催化剂 |
编号系统
CAS号:865-47-4
MDL号:MFCD00012162
EINECS号:212-740-3
RTECS号:暂无
BRN号:3556712
PubChem号:24884165
物性数据
1. 性状:白色粉末
2. 密度(g/mL,25/4℃):0.929
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):256-258°C
5. 沸点(ºC,常压):275°C。
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:未确定
8. 闪点(ºF):54 °F
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(220 °C):1 mm Hg
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:与水反应,在25~26 oC每100 g溶剂中的溶解度如下:己烷0.27 g,丙酮2.27 g,乙醚4.34 g,叔丁醇17.80 g,THF 25.00 g。
毒理学数据
暂无
生态学数据
对水是稍微有害的,不要让未稀释或大量的产品接触地下水,水道或者污水系统,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积23.1
7.重原子数量:6
8.表面电荷:0
9.复杂度:29
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:2
性质与稳定性
1.常温常压下稳定,避免氧化剂 水分接触
2.避免接触眼睛,皮肤和衣物;可以与水、氧气、二氧化碳反应。在高温下暴露于空气可能会导致燃烧。应在惰性气体盒或惰性气体包中进行操作。一般分成小份在氮气保护下密封保存。
3.极易吸湿,对皮肤粘膜有腐蚀性。通常是制成溶于叔丁醇的溶液。具强碱性。
贮存方法
储存在干爽的惰性气体下,保持容器密封,储存在阴凉,干燥的地方
合成方法
方法一在氮气保护下将1250毫升干燥的叔丁醇直接蒸馏入反应瓶中。分10次加入100克(2.6克原子)钾。搅拌的混合物立即发热,在15-60分钟内达到钾的熔点62C,此时金属分散成溶滴。当钾逐渐溶解时,混合物的温度上刃到叔丁醇的沸点。调节搅拌速度以保持叔丁醇稍稍回流。如果沸腾太剧烈,停止搅拌。必要时可将反应容器浸在冷的油浴中冷却(不能用水浴)。叔丁醇钾渐渐沉淀出来,当所有钾反应完后,混合物成为浓稠悬浮物。
方法二装在有密封搅拌器、氮气导入管(氮通过浓硫酸洗瓶和无水氯化钙干燥塔)、500毫升恒压滴液漏斗和回流冷凝器的3升三颈瓶中,放入用前新蒸的500毫升叔丁醇,加入20克(0.5克原子)清洁的金属钾。当钾反应完后,将回流冷凝器换成30厘米长的分馏柱。蒸去过量的叔丁醉直到溶液中出现晶体为止。加入2升干燥的庚烷,继续蒸馏直到柱顶温度达到98℃。残余物加干燥庚烷至1.5升。所得浆状物是叔一丁醇钾与叔丁醇的1:1络合物。在蒸汽浴上减压20-25mm以除去溶剂。可在氮气氛分中贮存几个月。
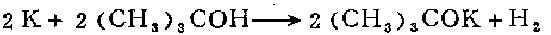
用途
1.作为强碱广泛应用于化工、医药、农药等有机合成中的缩合、重排和开环等反应中。还用于印染、催化剂等。
2.是一种有机合成中常用的强度适中的碱。其碱性强于碱金属的氢氧化物和碱金属的一级、二级醇盐;弱于氨基碱金属和它们的烷基衍生物。t-BuOK广泛使用的原因是它价廉易得,且它的碱性随所选的反应溶剂变化而变化。
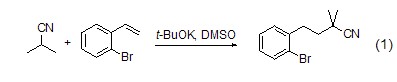
烷基化 t-BuOK的t-BuOH溶液可以有效地进行羰基α-位的烷基化反应。t-BuOK的t- BuOH溶液或苯溶液也常被用来进行α,β-双取代醛的烷基化。α,β-不饱和酮用过量的t-BuOK/t-BuOH和烷基化试剂处理,能够得到α,β-双烷基化的产物。催化剂量的t-BuOK在DMSO中可以催化酮或亚胺与苯乙烯的加成,得到高产率的烷基化产物 (式1)[1]。
与分子间反应相比,t-BuOK在不同溶剂中都能催化分子内烷基化。α,β-不饱和酮的分子内烷基化可以在α-, α2-或者γ-位发生,这取决于碱的特点、离去基团以及其它结构特征 (式2)[2]。
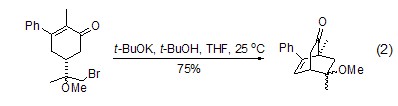
缩合反应 t-BuOK是Darzens缩合反应最常用的碱。Darzens缩合是α-卤代酯与酮、芳醛生成α,β-环氧或缩水甘油酸酯的反应 (式3)[3]。

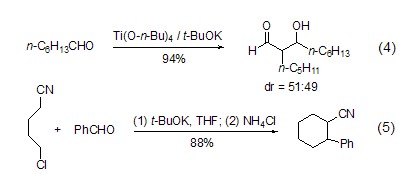
二酯的Dieckmann环化及其相关反应在五元、六元、七元和更大环的合成中有广泛的应用[4]。在不对称体系中,空间效应和产物烯醇化物的稳定性决定了反应的区域选择性。碱的性质也能显著影响这个反应的区域选择性。对Stobbe缩合来说,t-BuOK是比EtONa更好的碱,反应产率更高,反应时间更短,而且没有酮或者醛还原的副反应。Ti(O-n-Bu)4和t-BuOK以1:1形成的混合试剂能够有效地催化醛的自缩合反应,但是立体选择性不高 (式4) [5]。氧杂环腈可以由ω-卤代腈在t-BuOK作用下发生缩合反应得到 (式5)[6]。
消除反应 t-BuOK无论在α-消除还是β-消除中都有广泛的应用。它是传统的生成二卤代卡宾的醇盐-卤仿反应的最有效的碱 (式6)[7]。底物含有烷基氯、溴、甲苯磺酸酯、亚磺酸酯等离去基团时,在t-BuOH或其它非极性溶剂中t-BuOK的作用下可以进行β-消除, 此反应也可以在固相中进行。

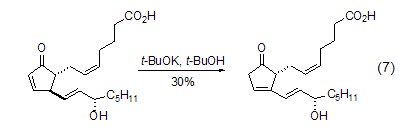
不饱和化合物的异构化 t-BuOK能使烯烃和炔烃双键通过负离子中间体迁移 (式7)[8]。
Michael加成 t-BuOK还可以用作Michael加成反应中的碱。不对称酮 (如2-甲基环己酮) 的Michael加成产物主要是在更多取代基的α-碳原子上。1,2-丙二烯酮在t-BuOK作用下可以与1,3-二羰基化合物发生Michael加成反应,产率较高 (式8)[9]。

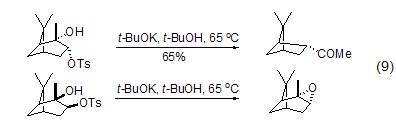
重排反应 顺式1,2-二醇的单对甲苯磺酸化衍生物,比如α-蒎烯衍生物,在t-BuOK作用下经历了Pinacol重排过程。反式异构体在相同的条件下转化为环氧化物 (式9)[10]。α-卤代砜的Ramberg-Backlund重排也可以用t-BuOK来催化。
安全信息
危险运输编码:UN 3206 4.2/PG 2
危险品标志: 易燃
易燃  腐蚀
腐蚀
安全标识:S16 S26 S43 S45 S36/S37/S39
文献
1. Rodriguez, A. L.; Bunlaksananusorn, T.; Knochel, P. Org. Lett., 2000, 2, 3285. 2. Srikrishna, A.; Hemamalini, P.; Sharma, G. V. R. J. Org. Chem., 1993, 58, 2509. 3. Trost, B. M.; Fleming, I. Comprehensive Organic Synthesis, Pergamon Press: Oxford, 1991, Vol.2, p 409. 4. Davis, B. R.; Garratt, P. J. Comprehensive Organic Synthesis, Pergamon Press: Oxford, 1991, Vol. 2, 795. 5. Han, Z. F.; Yorimitsu, H.; Shinokubo, H.; Oshima, K. Tetrahedron Lett., 2000, 41, 4415 6. Fleming, F. F.; Gudipati, V.; Steward. O. W. J. Org. Chem., 2003, 68, 3943. 7. Taylor, R. T.; Paquette, L. A.Org. Synth. Coll. Vol. VII, 1990, 200. 8. Corey E. J.; Cyr, C. R. Tetrahedron Lett., 1974, 1761. 9. Ma, S.; Yu, S. C.; Qian, W. J. Tetrahedron, 2005, 61, 4157 10. Carlson, R. G.; Pierce, J. K. Tetrahedron Lett., 1968, 6213. 11.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无







 沪公网安备 31010602001115号
沪公网安备 31010602001115号