| 物竞编号 | 1D5T |
|---|---|
| 分子式 | C3H5N3O2 |
| 分子量 | 115.07 |
| 标签 | 乙氧基衍生物 |
编号系统
CAS号:817-87-8
MDL号:暂无
EINECS号:暂无
RTECS号:暂无
BRN号:暂无
PubChem号:暂无
物性数据
1.沸点(℃,30.5 mmHg):40
2.溶解性:溶于乙醚、二氯甲烷。
毒理学数据
暂无
生态学数据
暂无
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):1.8
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:2
5.互变异构体数量:无
6.拓扑分子极性表面积40.7
7.重原子数量:8
8.表面电荷:0
9.复杂度:127
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:1
15.共价键单元数量:1
性质与稳定性
叠氮甲酸乙酯可用在两类反应中:(a) 叠氮化物与不饱和官能团的环加成反应;(b) 用来制备乙氧羰基氮卡宾。因为其热力学不稳定性,所以它在合成中的应用有限。叠氮甲酸乙酯和其它叠氮乙酯在60 ℃ 以上会发生分解。
氮杂环丙烷的合成 叠氮化物对烯烃的环加成反应是重要的。叠氮甲酸乙酯是缺电子的,容易与富电子的烯烃反应。这些反应的产物是三唑啉,在更高温度下,三唑啉也容易分解,生成氮杂环丙烷。叠氮甲酸乙酯热分解生成单线态乙氧羰基氮卡宾,乙氧羰基氮卡宾也与烯烃反应生成氮杂环丙烷 (式1)[2]。
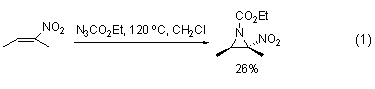
叠氮甲酸乙酯还能与不活泼的烯烃和富含烯键的单层碳纳米管反应[3,4],形成氮杂环丙烷。而在此反应条件下,会生成氮卡宾等。
二亚胺的合成 叠氮甲酸乙酯还可以与二硫酮发生反应得到相应的二亚胺。这个反应产率很高。可能的机理是叠氮基与硫羰基发生1,3-偶极环加成,然后失去N2形成硫杂、氮杂环丙烷,再在二硫环上的硫原子作用下得到亚胺 (式2) [5,6]。
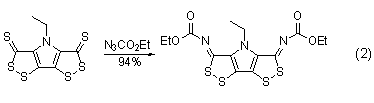
光解反应与氮卡宾的生成 光解叠氮甲酸乙酯生成乙氧羰基氮卡宾。生成的氮卡宾既可以以单线态形式反应,也可以以三线态反应,并且有不同的反应活性。在光解条件下,氮卡宾对双键的加成有广泛应用。单线态氮卡宾对烯烃的加成有立体专一性,这个反应可以用于很多种类的烯烃中而生成亚胺类化合物。乙氧羰基氮卡宾与活性很低的环丁烯砜反应生成二乙烯基氨基甲酸酯。乙氧羰基氮卡宾也可以与活性烯烃反应,如与烯基醚4,5-二氢呋喃衍生物 (式3)[7] 反应。该反应有较好的立体选择性,水的加入和低压紫外灯的使用是提高产率的关键。乙氧羰基氮卡宾也可与链式烯加成生成相应的化合物 (式4)[8],许多光解反应可以在室温下进行以减少副反应的发生。
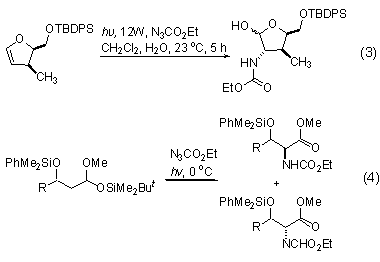
在光解条件下,叠氮甲酸乙酯对双键的加成形成氮杂环丙烷 (式5)[9,10]。
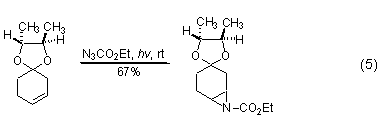
另外,乙氧羰基氮卡宾也可与一系列其它类型化合物反应,如与二苯乙炔反应生成唑。在光解条件下,乙氧羰基氮卡宾与脂肪族腈生成相应的5-乙氧基恶二唑。叠氮甲酸乙酯与1,1-二甲基丙二烯在光解条件下反应生成唑啉,乙氧羰基氮卡宾与异氰化物发生光化学加成生成相应的碳二亚胺,产率适中,碳二亚胺可以水解生成脲。乙氧羰基氮卡宾还可以与钴环戊二烯络合物加成生成吡咯,但产率很低。
贮存方法
在蒸馏或加热时有爆炸危险。在阴凉、避光处保存三个月以上不会明显降解;而在潮湿的条件下容易水解成氨气。长期保存的叠氮甲酸乙酯可生成氨气,容易爆炸,建议现用现制。叠氮甲酸乙酯蒸气有毒,使用时应在通风橱中进行。
合成方法
通过氯甲酸乙酯与叠氮化钠反应制备,该方法由Wlater和Mattingly[1]报道。
用途
与苯反应制备N-碳乙氧基氮杂草,与苯乙炔或乙氧基乙炔反应制备1-碳乙氧基三唑及其乙氧基衍生物等。
安全信息
危险运输编码:暂无
危险品标志:暂无
安全标识:暂无
危险标识:暂无
文献
1. Walter, L.; Mattingly, J.; Thomas, W.; J. Am. Chem. Soc., 1965, 87, 1947 2. Fioravanti, S.; Pellacani, L.; Stabile, S.; Tardella, P. A.; Ballini, R. Tetrahedron, 1998, 54, 6169. 3. Holzinger, M.; Abraham, J.; Whelan, P.; Graupner, R.; Ley, L.; Hennrich, F.; Kappes, M.; Hirsch, A. J. Am. Chem. Soc., 2003, 125, 8566. 4. Michael, H.; Otto, V.; Andreas, H.; Frank, H.; Manfred, K.; Robert, W.; Frank, J. Angew. Chem., Int. Ed., 2001, 40, 4002. 5. Marcos, C. F.; Polo, C.; Rakitin, O. A.; Rees, C. W.; Torroba, T. Chem. Commum., 1997, 879. 6. Fuertes, P.; Marcos, C. F.; Miguel, D.; Ratikin, O. A.; Rees. C. W.; Torroba, T.; Barriga, S. J. Org. Chem., 2001, 66, 5766. 7. Williams, D. R.; Rojas, C. M.; Bogen, S. L. J. Org. Chem., 1999, 64, 736. 8. Loreto, M. A.; Tardella, P. A.; Tedeschi, L.; Tofani, D. Tetrahedron Lett., 1997, 38, 5717. 9. Fioravanti, S.; Luna, G.; Pellacani, L.; Tardella, P. A. Tetrahedron, 1997, 53, 4779. 10. Buron, C.; Platz, M. S. Org. Lett., 2003, 5, 3383. 11.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号