| 物竞编号 | 05FD |
|---|---|
| 分子式 | C7H6N4O |
| 分子量 | 162.15 |
| 标签 | 1,1'-羰基二咪唑, 1,1'-羰二咪唑, 羰基二咪唑, 1,1′-Carbonyldiimidazole, Carbonyldiimidazole, N,N'-Carbonyldiimidazole, CDI, CO(Im)2, 偶联剂, 酶·蛋白质·肽, 肽合成用, 酰化试剂 |
编号系统
CAS号:530-62-1
MDL号:MFCD00005286
EINECS号:208-488-9
RTECS号:暂无
BRN号:6826
PubChem号:暂无
物性数据
1. 性状:白色晶体
2. 密度(g/ cm3,25/4℃):未确定
3. 相对蒸汽密度(g/cm3,空气=1):未确定
4. 熔点(ºC):117~122
5. 沸点(ºC,常压):未确定
6. 沸点(ºC,8kPa):未确定
7. 折射率:未确定
8. 闪点(ºF):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,55.1ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶于极性有机溶剂,通常在CH2Cl2、THF或者乙腈中使用。
毒理学数据
暂无
生态学数据
该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
1、 摩尔折射率:44.57
2、 摩尔体积(cm3/mol):116.4
3、 等张比容(90.2K):328.4
4、 表面张力(dyne/cm):63.2
5、 极化率(10-24cm3):17.67
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积52.7
7.重原子数量:12
8.表面电荷:0
9.复杂度:166
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.按规格使用和贮存,不会发生分解,避免与氧化物接触。
2.对湿气非常敏感,建议在干燥阴凉处储存。
贮存方法
储存于阴凉、干燥、通风良好的库房。远离火种、热源。防止阳光直射。包装密封。应与酸类、食用beplay体育首页 分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
1.将咪唑与溶于苯的光气反应,滤除反应物中的咪唑盐酸盐,滤液浓缩至干,得1,1'-羰基二咪唑,产率91%。
2.注意!光气有毒,此操作应在通风橱中进行
将200毫升无水苯注入一个已校准的500毫升锥形漏斗中,加塞子并称重。取下玻璃塞,在漏斗上安装一支带砂芯过滤器的气体导入管。在室温和干燥管保护下,在约1小时内通入光气巧一20克(苯溶液体积相应增加约12一16毫升)。塞好漏斗,立即称重,算出实际通入光气的重量为16.55克(0.167摩尔)、由此,按光气与咪哇的摩尔比为1:4以计算出所需的咪些量。然后,将此漏斗安装在一个1升的,内盛有按计算所需的45.60的克(0.669摩尔)咪哇和500毫升无水四氢吠喃的三颈烧瓶上。在冷水冷却和电磁搅拌下,于15-30分钟内滴加光气的苯溶液。继续搅拌15分钟后,在室温下静置1小时。在隔绝潮气下,用砂芯漏斗滤除味哇盐酸盐。滤液在40一50℃和减压下浓缩至干,得无色结晶24。S克(91%)。在110℃熔结,其纯度足可以用于许多反应(如醋、肤和醛的合成中)。
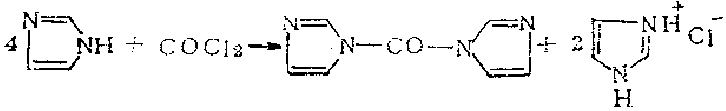
3.可以按照标准的实验步骤以光气和咪唑为原料来制备[1]。
用途
N,N-碳酰二咪唑 (CDI) 在有机合成中主要被用作甲酰基转移试剂和羧酸的活化试剂。由于该试剂反应活性高、廉价和反应后处理简单,比同类试剂DCC和EDC具有更高的应用价值。
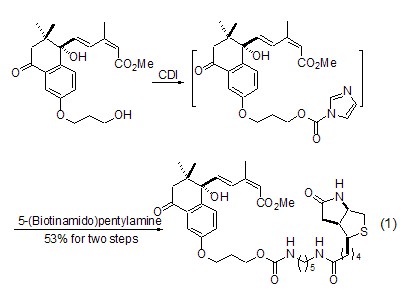
CDI分子中的碳酰基受到咪唑的活化而具有非常高的甲酰化反应活性。该试剂遇到带有活性氢的羟基或者氨基后,根据反应的条件可以同时失去二个咪唑生成碳酰衍生物[2],也可以失去一个咪唑生成N-咪唑甲酰酯或者N-咪唑甲酰胺。生成的N-咪唑甲酰化合物可以发生进一步的反应,将另一个咪唑置换出去,生成具有不对称结构的碳酰衍生物 (式1)[3]。
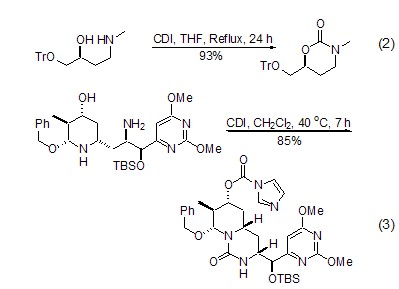
使用带有二个活性氢官能团的底物与CDI作用,则可以发生分子内的碳酰化反应得到环状产物。二个活性氢官能团相同 (式2)[4,5]或者不同 (式3)[6]的底物都给出非常满意的结果。
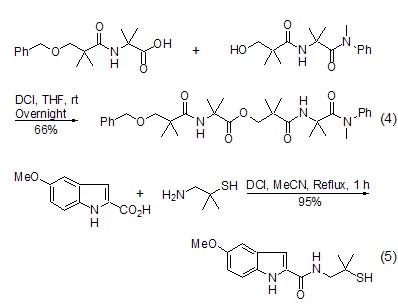
如果带有活性氢官能团的底物是羧酸,则生成相应的酰基咪唑,从而使得该羧酸的酰基被活化。酰基咪唑与醇或者胺可在非常温和的条件下生成相应的羧酸酯 (式4)[7,8] 或者酰胺 (式5)[9]。该过程实际上是一个两步反应,但是大多数情况下可以用“一锅煮”的步骤来完成。合成酰胺的反应特别有意义,因为可以有效地应用于多肽的合成[10]。有文献报道,CO2可以催化加速酰胺化反应的速度[11,12]。
安全信息
危险运输编码:UN 3263 8/PG 2
危险品标志: 腐蚀
腐蚀
安全标识:S26 S45 S36/S37/S39
文献
1. Staab, H. A.; Wendel, K. Org. Synth., 1968, 48, 44. 2. Kishikawa, K.; Nakahara, S.; Nishikawa, Y.; Kohmoto, S.; Yamamoto, M. J. Am. Chem. Soc., 2005, 127, 2565. 3. Nyangulu, J. M.; Galka, M. M.; Jadhav, A.; Gai, Y.; Graham, C. M.; Nelson, K. M.; Cutler, A. J.; Taylor, D. C.; Banowetz, G. M.; Abrams, S. R. J. Am. Chem. Soc., 2005, 127, 1662. 4. White, J. D.; Hansen, J. D. J. Org. Chem., 2005, 70, 1963. 5. Davis, F. A.; Deng, J. Org. Lett., 2004, 6, 2789. 6. Grant, E. B.; Weiss, J. M.; Branum, S.; Hayden, S.; Johnson, S.; Guiadeen, D.; Murray, W. V.; Macielag, M. J. Tetrahedron Lett., 2005, 46, 2731. 7. Ella-Menye, J.-R.; Sharma, V.; Wang, G. J. Org. Chem., 2005, 70, 463. 8. Dandapani, S.; Curran, D. P. J. Org. Chem., 2004, 69, 8751. 9. Iliev, B.; Linden, A.; Heimgartner, H. Helv. Chim. Acta, 2003, 86, 3215. 10. Schlosser, K. M.; Krasutsky, A. P.; Hamilton, H. W.; Reed, J. E.; Sexton, K. Org. Lett., 2004, 6, 819. 11. Pedras, M. S. C.; Chumala, P. B.; Quail, J. W. Org. Lett., 2004, 6, 4615. 12. Vaidyanathan, R.; Kalthod, V. G.; Ngo, D. P.; Manley, J. M.; Lapekas, S. P. J. Org. Chem., 2004, 69, 2565. 13.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无







 沪公网安备 31010602001115号
沪公网安备 31010602001115号