| 物竞编号 | 01HX |
|---|---|
| 分子式 | C2H4O |
| 分子量 | 44.05 |
| 标签 | 无水乙醛, 醋醛, Methanecarbaldehyde, Ethanal, Acetic aldehyde, 醛类溶剂, 脂肪族化合物 |
编号系统
CAS号:75-07-0
MDL号:MFCD00006991
EINECS号:200-836-8
RTECS号:AB1925000
BRN号:505984
PubChem号:24844966
物性数据
1.性状:无色液体,有强烈的刺激臭味。[1]
2.熔点(℃):-123.5[2]
3.沸点(℃):20.8[3]
4.相对密度(水=1):0.788(16℃)[4]
5.相对蒸气密度(空气=1):1.52[5]
6.饱和蒸气压(kPa):98.64(20℃)[6]
7.燃烧热(kJ/mol):-1166.37[7]
8.临界温度(℃):188[8]
9.临界压力(MPa):6.4[9]
10.辛醇/水分配系数:0.43[10]
11.闪点(℃):-39(CC);-40(OC)[11]
12.引燃温度(℃):175[12]
13.爆炸上限(%):57[13]
14.爆炸下限(%):4.0[14]
15.溶解性:溶于水,可混溶于乙醇、乙醚、苯、汽油、甲苯、二甲苯等。[15]
16.临界密度(g·cm-3):0.286
17.临界体积(cm3·mol-1):154
18.Lennard-Jones参数(A):11.98
19.Lennard-Jones参数(K):141.3
20.溶度参数(J·cm-3)0.5:19.819
21.van der Waals面积(cm2·mol-1):4.490×109
22.van der Waals体积(cm3·mol-1):28.810
23.液相标准燃烧热(焓)(kJ·mol-1):-1165.79
24.液相标准声称热(焓)( kJ·mol-1):-192.88
25.液相标准熵(J·mol-1·K-1) :117.3
26.液相标准热熔(J·mol-1·K-1):89.05
27.气相标准燃烧热(焓)(kJ·mol-1):-1192.48
28.气相标准声称热(焓)( kJ·mol-1) :-166.19
29.气相标准熵(J·mol-1·K-1) :263.95
30.气相标准生成自由能( kJ·mol-1):-133.0
31.气相标准热熔(J·mol-1·K-1):55.32
毒理学数据
1.急性毒性[16]
LD50:661mg/kg(大鼠经口)
LC50:13300ppm(大鼠吸入,4h)
2.刺激性[17]
家兔经皮:500mg,轻度刺激(开放性刺激试验)
家兔经眼:40mg,重度刺激。
3.亚急性与慢性毒性[18] 大鼠、豚鼠经口给予100mg/kg可以耐受6个月,出现反射活动障碍,动脉压升高;经口给予10mg/kg,2~3个月也可引起同样的改变。
4.致突变性[19] 微生物致突变:鼠伤寒沙门菌7880μg/皿。姐妹染色单体交换:人淋巴细胞40μmol/L。DNA损伤:人淋巴细胞1560μmol/L。DNA抑制:人HeLa细胞10mmol/L。姐妹染色单体交换:人淋巴细胞1200μmol/L。
5.致畸性[20] 大、小鼠孕后不同时间经口或腹腔内给予最低中毒剂量(TDLo),致呼吸系统、肝胆管系统、中枢神经系统、内分泌系统、泌尿生殖系统、肌肉骨骼系统、颅面部(包括鼻、舌)发育畸形。
6.致癌性[21] IARC致癌性评论:G2B,可疑人类致癌物。
7.其他[22] 小鼠静脉最低中毒剂量(TDLo):120mg/kg(孕后7~9d用药),胚泡植入后死亡率增高,对胎鼠有毒性。
生态学数据
1.生态毒性[23]
LC50:37.2mg/L(96h)(黑头呆鱼);53mg/L(96h)(蓝鳃太阳鱼)
EC50:42mg/L(48h)(水蚤);30.8mg/L(96h)(黑头呆鱼)
2.生物降解性[24] MITI-I测试,初始浓度100ppm,污泥浓度30ppm,2周后降解80%。
3.非生物降解性[25] 空气中,当羟基自由基浓度为5.00×105个/cm3时,降解半衰期为24h(理论)。
大气中光解半衰期8.4~16h
分子结构数据
1、摩尔折射率:11.50
2、摩尔体积(cm3/mol):58.8
3、等张比容(90.2K):120.6
4、表面张力(dyne/cm):17.6
5、极化率(10-24cm3):4.55
计算化学数据
1.疏水参数计算参考值(XlogP):-0.3
2.氢键供体数量:0
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:2
6.拓扑分子极性表面积17.1
7.重原子数量:3
8.表面电荷:0
9.复杂度:10.3
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.化学性质:活泼,分子中的羰基易进行加成、环化和聚合反应。易氧化成乙酸。在水中可形成水合物。遇明火、高热极易燃烧爆炸。
2.乙醛为易燃有毒液体。对眼、皮肤和呼吸器官有刺激作用。轻度中毒会引起气喘、咳嗽及头痛等症状,重者会引起肺炎及脑膜炎。长期接触会引起红细胞降低、血压升高。小鼠灌胃LD50:1232mg/kg。操作现场空气中最高容许浓度200*10-6。操作人员必须穿戴好劳动保护用具。
3.蒸气与空气形成爆炸性混合物,爆炸极限4.1%~57.0%(体积)。
4.稳定性[26] 稳定
5.禁配物[27] 强酸、强氧化剂、强还原剂、强碱、卤素、氧、易燃物、氨、硫化氢、磷、胺类、醇、酮、酐、酚等
6.避免接触的条件[28] 受热、接触空气
7.聚合危害[29] 聚合
贮存方法
储存注意事项[30] 储存于阴凉、通风的库房。远离火种、热源。库温不宜超过29℃。包装要求密封,不可与空气接触。应与氧化剂、还原剂、酸类等分开存放,切忌混储。不宜大量储存或久存。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。
合成方法
乙醛有多种生产方法:
1.乙烯直接氧化法 乙烯和氧气通过含有氯化钯、氯化铜、盐酸及水的催化剂,一步直接氧化合成粗乙醛,然后经蒸馏得成品。
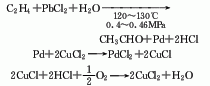
2.乙醇氧化法 乙醇蒸气在300-480℃下,以银、铜或银-铜合金的网或粒作催化剂,由空气氧化脱氢制得乙醛。
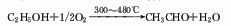
3.乙炔直接水合法 乙炔和水在汞催化剂或非汞催化剂作用下,直接水合得到乙醛。因有汞害问题,已逐渐为他法取代。
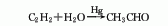
4.乙醇脱氢法 在添加钴、铬、锌或其他化合物的铜催化剂作用下,乙醇脱氢生产乙醛。
5.饱和烃类氧化法。
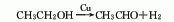
原料消耗定额:乙炔水合法每吨产品消耗99%乙炔610kg;乙醇氧化法消耗95%乙醇1200kg;乙烯氧化法(一步法)消耗99%乙烯710kg,氧气(99%)300立方米。市售工业品乙醛,乙烯法乙醛纯度为99.7%,乙醇法纯度为98%。
6.制法:
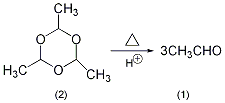
于装有分馏装置(接受瓶用冰浴冷却,以减少乙醛的挥发损失)的反应瓶中,加入多聚乙醛(2)50g,浓硫酸0.5mol,几粒沸石。慢慢加热,注意不要使分馏柱顶端的温度过于32℃。反应应缓慢的进行,因为乙醛和多聚乙醛可形成共沸物,bp42℃(摩尔比为乙醛:多聚乙醛=53.4:46.6)。大部分的乙醛(1)于21~25℃蒸出。当反应瓶中大约剩余10mL时停止蒸馏(若蒸馏至干有爆炸的危险)。这样制备的乙醛能满足大多数用途。若需要纯度更高的乙醛,可重新进行分馏,收集21℃的馏分。[32]
7.制法:
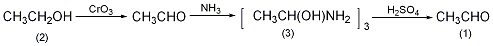
于装有通气导管、滴液漏斗、蒸馏装置(接受瓶可用两个依次相连的洗气瓶,内盛乙醚,并用冰盐浴冷却)的反应瓶中,加入乙醇(2)135mL(约2mol),加入1/3体积的由150mL浓硫酸与250mL水配成的稀硫酸。通入二氧化碳气体,加热至沸。将另外2/3体积的硫酸用100mL水稀释后,加入200g重铬酸钠,搅拌溶解,滴加此溶液至反应物中,反应放热。生成的乙醛不断被二氧化碳气流带出,乙醛溶于乙醚中。约30min滴完,而后继续通二氧化碳10min。得到乙醛的乙醚溶液。乙醛不能从其乙醚溶液中蒸馏出来。若得到纯的乙醛,可按如下方法进行:将乙醛的乙醚溶液用冰水浴冷却,慢慢通入干燥的氮气,不断摇动。其间析出乙醛胺结晶,直至析出完全①。抽滤,无水乙醚洗涤,干燥,得乙醛胺(3)55g。于装有通气导管、滴液漏斗、蒸馏装置(接受瓶用冰盐浴冷却)的反应瓶中,加入化合物(3),用50mL水溶解,通入二氧化碳气体,水浴加热,滴加由60mL浓硫酸和80mL水配成的稀硫酸,生成的乙醛不断蒸出,约30min滴完,乙醛的沸点21℃。注:①取少量透明液,通入氮气至饱和,若无沉淀析出,则表明反应结束。[33]
用途
1.比色法测定醛时用以制备标准溶液、还原剂、杀菌剂。制造多聚乙醛、乙酸、丁醇季戊四醇。有机合成中间体、溶剂。
2.工业上用以制造多聚乙醛、醋酸、乙酸乙酯、季戊四醇、塑料、合成橡胶、合成树脂等。也可用于分光光度法测定醛。
3.还原剂,杀菌剂,比色法测定醛时用以制备标准溶液。工业上用以制造多聚乙醛、乙酸、合成橡胶等。
4.用于制造醋酸、醋酐和合成树脂。[31]
安全信息
危险运输编码:UN 1089 3/PG 1
危险品标志: 很易燃
很易燃  有害
有害
文献
[1~31]参考书:危险beplay体育首页 安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8 [32]参考文献:Furniss B S,Hannaford A J,Rogers V,et al. Vogel’s Texbook of Practical Chemistry. Longman London and New YorK. Fourth edition,1978:325. 参考书:有机化合物合成手册/孙昌俊,王秀菊,孙风云主编. 北京:化学工业出版社,2011.8 ISBN 978-122-11519-54. Cueto R, Pryor W A. Vib. Spectr., 1994, 7: 97-111. [33]参考文献:参考书:有机化合物合成手册/孙昌俊,王秀菊,孙风云主编. 北京:化学工业出版社,2011.8 ISBN 978-122-11519-5
备注
暂无







 沪公网安备 31010602001115号
沪公网安备 31010602001115号