| 物竞编号 | 0FKQ |
|---|---|
| 分子式 | C43H72Cl2P2Ru |
| 分子量 | 822.96 |
| 标签 | 第I代Grubbs 催化剂, Grubbs Catalyst 1st Generation, 催化剂 |
编号系统
CAS号:172222-30-9
MDL号:MFCD01090946
EINECS号:暂无
RTECS号:暂无
BRN号:暂无
PubChem号:暂无
物性数据
1. 性状:紫红色粉末状固体
2. 密度(g/mL,25℃):未确定
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):153
5. 沸点(ºC,常压):未确定
6. 沸点(ºC,8mmHg):未确定
7. 折射率(n20/D):未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(mmHg,217ºC):未确定
12. 饱和蒸气压(kPa,25ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:易溶于有机溶剂,通常在CH2Cl2、苯或者甲苯的溶液中使用。
毒理学数据
暂无
生态学数据
暂无
分子结构数据
暂无
计算化学数据
暂无
性质与稳定性
该试剂对空气和湿气较稳定,即使放置在空气中也不会分解,其催化活性也不受到溶剂中空气、水蒸气以及痕量杂质的影响。
贮存方法
密封储存,储存于阴凉、干燥的库房。冷藏温度4ºC。
合成方法
实验室可以参考文献的标准实验步骤来制备[1,2]。
用途
Grubbs催化剂 (第I代) 是一个物理性质和化学性质比较稳定的“烯烃复分解反应”的标准催化剂。自从1992年Grubbs 小组[1,2]报道该试剂以后,它在有机合成中的应用已经非常广泛,是含有多种官能团的不饱和碳环和杂环的重要合成方法,许多文献对该试剂的性质和应用进行了非常详细的综述[3~7]。
Grubbs催化剂参与的金属复分解反应的机理实际上是金属卡宾参与的碳骨架重排反应。含有两个烯键的分子在催化剂的参与下发生复分解反应,伴随着失去一分子烯烃,同时形成新的分子间或者分子内烯烃。第I代Grubbs催化剂的化学选择性高,但反应活性较低。因此,大多情况下催化剂的用量在5%摩尔以上,有时必须使用高达50% 的摩尔用量才能得到满意的结果。
Grubbs催化剂可以选择性地使双键和三键发生复分解反应,而对大多数其它官能团不产生明显的影响,是一个适用范围非常广泛的试剂。例如:它可以催化分子间的复分解反应,主要得到两分子交叉复分解的产物。同时,又可以很好地兼容底物分子中的羟基和酯基 (式1,式2)[5],这是Schrock催化剂所不具备的特点。
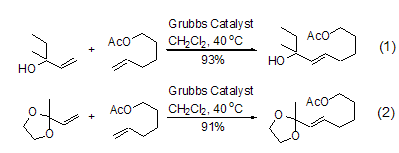
Grubbs 催化剂的特征反应类型是催化含有两个双键的底物分子发生分子内“成环复分解反应”(RCM Reaction)。该反应条件温和简单,一般只需将底物与催化剂在CH2Cl2、苯或者甲苯的溶液中室温下或者加热搅拌数小时即可完成。在大多数情况下,反应产物单一,产率维持在中等偏上的水平,有时可达到几乎定量的水平。“成环复分解反应”常常被用于大环天然产物全合成中的关键步骤,使得复杂的合成变的异常简单 (式3)[8]。
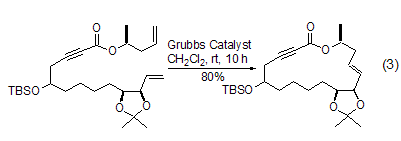
Grubbs 催化剂还被成功地用于含氮杂环类天然产物的合成。直接使用游离的仲胺和叔胺会导致产率较低,提高产率的简单方法是将它们转化为相应的酰胺或者季铵盐 (式4)[9]。
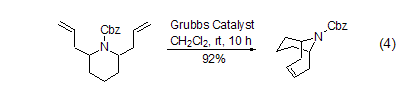
第1代Grubbs催化剂一般不适用于含硫底物的反应,可能的原因是底物分子中硫原子参与了催化剂中金属原子的配位,导致催化剂活性降低。例如:二烯丙基硫醚的“成环复分解反应”收率只有29% (式5)[10]。
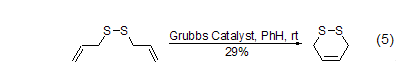
安全信息
危险运输编码:暂无
危险品标志: 刺激
刺激
危险标识:R36/37/38
文献
1. Fu, G. C.; Nguyen, S. T.; Grubbs, R. H. J. Am. Chem. Soc., 1993, 115, 9856. 2. Nguyen, S. T.; Grubbs, R. H.; Ziller, J. W. J. Am. Chem. Soc., 1993, 115, 9858. 3. Fürstner, A. Angew. Chem. Int. Ed., 2000, 39, 3012. 4. Grubbs, R. H.; Chang, S. Tetrahedron, 1998, 54, 4413. 5. Arnab, K.; Grubbs, R. H. J. Am. Chem. Soc., 2003, 125, 11360. 6. Deiters, A.; Martin, S. F. Chem. Rev., 2004, 104, 2199. 7. Nicolaou, K. C.; Bulger, P. G.; Sarlah. D. Angew. Chem. Int. Ed., 2005, 44, 4490. 8. Geng, X; Danishefsky, S. J. Org. Lett., 2004, 6, 413. 9. Neipp, C. E.; Martin, S. F. J. Org. Chem., 2003, 68, 8867. 10. Shon, Y. S.; Lee, T. R. Tetrahedron Lett., 1997, 38, 1283. 11.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无





 沪公网安备 31010602001115号
沪公网安备 31010602001115号