| 物竞编号 | 0CZD |
|---|---|
| 分子式 | C4H9ClO2 |
| 分子量 | 124.57 |
| 标签 | 1-氯甲基-2-甲氧基乙烷, 1-Chloromethoxy-2-methoxyethane, β-Methoxyethoxymethyl chloride, MEM-chloride, MEMCl, 羟基保护剂 |
编号系统
CAS号:3970-21-6
MDL号:MFCD00000888
EINECS号:223-589-8
RTECS号:暂无
BRN号:1900576
PubChem号:24861920
物性数据
1.性状:无色液体
2.密度:1.091g/cm3
3.沸点:(oC/13 mmHg):50-52
4.溶解性:溶于大多数有机溶剂,通常在CH2Cl2, THF和DMF 中使用。
毒理学数据
生态学数据
通常对水是不危害的,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):0.6
2.氢键供体数量:0
3.氢键受体数量:2
4.可旋转化学键数量:4
5.互变异构体数量:无
6.拓扑分子极性表面积18.5
7.重原子数量:7
8.表面电荷:0
9.复杂度:32.9
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
对湿气敏感,带有刺激性味道。建议在通风橱中操作,在无水体系中使用。
贮存方法
-20℃ ,避光,通风干燥处,密封保存
合成方法
1. 实验室可以2-甲氧基乙醇和甲醛在HCl的存在下制备[1]。
2. 在搅拌下将15克甲氧基乙醇和66克三聚甲醛,用干燥氯化氢处理,直到反应混合物变得清亮。此时用900毫升戊烷稀释,并用100克硫酸镁在5℃干燥3小时。蒸出戊烷,留下MEMCI,产率90%。将MEMC1的乙醚溶液与}.}当量三乙胺在25℃反应16小时,生成无色晶体钱盐。过滤。在真空中干燥,得纯产品,产率约80%。mp58一61℃。在密闭容器中是稳定的,但必须防止空气中的水蒸气。
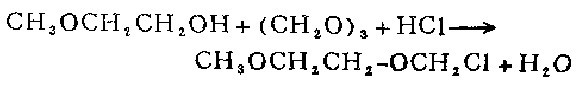
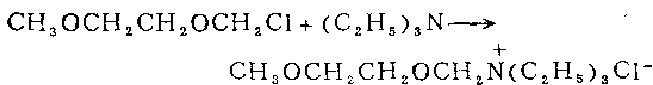
用途
1、用作罗红霉素的中间体。
2、1-氯甲氧基-2-甲氧基乙烷 (MEMCl) 被定义为有机合成中的重要保护基。它可以在温和的条件下与羟基、氨基和羧酸反应生成相应的醚、取代胺和酯,生成的产物也可以在多种条件下脱去保护基。
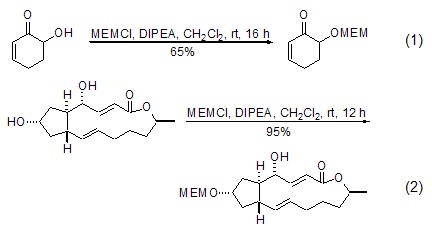
MEMCl与醇羟基反应生成相应的MEM 醚特别重要。与MOM保护基的生成相比较,它的生成条件更容易。虽然早期有许多碱催化剂被用于MEM的生成反应,但现在绝大多数情况下可以使用同一个简单的标准实验条件:用i-Pr2NEt为碱催化剂,将MEMCl与底物分子在CH2Cl2溶液中室温下搅拌若干个小时即可 (式1)[2]。有时MEMCl与底物分子中多个醇羟基的反应具有一定的区域选择性 (式2)[3,4]。
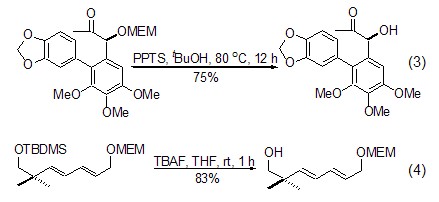
MEM保护基的重要性还体现在它的脱保护性质上。目前较常使用的脱保护方法主要有PPTS-tBuOH 或者TiCl4-CH2Cl2体系 (式3)[5,6]。由于该保护基对多种脱保护试剂具有一定的稳定性,可以在多种保护基共存下实现选择性去保护 (式4)[7,8]。
MEMCl与酚羟基反应生成相应的MEM醚,一般情况下NaH被用作碱 (式5)[9,10]。文献报道,MEMCl和含有酚羟基和醇羟基的底物分子反应时,选择性主要来自于苯环上取代基的影响[11]。MEMCl与带有活性氢的酰胺反应条件与酚类似,生成N-MEM(式6)[12,13]。它们脱保护的条件也非常类似,常用的方法是将底物在aq. HCl-MeOH或者TFA溶液中加热或者回流。
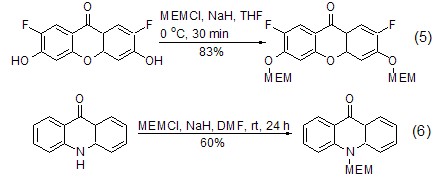
MEMCl与羧酸反应生成相应的酯,可以选用醇羟基的反应条件,以i-Pr2NEt为碱催化剂,也可以选用无机碳酸盐为碱催化剂 (式7)[14,15]。使用aq. HCl-MeOH和TFA在室温下即可实现脱保护反应。
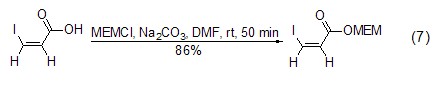
安全信息
危险运输编码:UN 2810 6.1/PG 2
危险品标志: 有毒
有毒
安全标识:S26 S45 S53 S36/S37/S39
文献
1. Zupancic, B. G.; Sopcic, M. Synthesis, 1982, 942. 2. Hong, S.-p.; Lindsay, H. A.; Yaramasu, T.; Zhang, X.; McIntosh, M. C. J. Org. Chem., 2002, 67, 2042. 3. Suh, Y.-G.; Jung, J.-K.; Seo, S.-Y.; Min, K.-H.; Shin, D.-Y.; Lee, Y.-S.; Kim, S.-H.; Park, H.-J. J. Org. Chem., 2002, 67, 4127. 4. Wipf, P.; Soth, M. J. Org. Lett., 2002, 4, 1787. 5. Gurjar, M. K.; Cherian, J.; Ramana, C. V. Org. Lett., 2004, 6, 317. 6. Andres, J. M.; Elena, N. de; Pedrosa, R.; Perez-Encabo, A. Tetrahedron: Asymmetry, 2001, 12, 1503. 7. Richter, F.; Bauer, M.; Perez, C.; Maichle-Mossmer, C.; Maier, M. E. J. Org. Chem., 2002, 67, 2474. 8. Andrus, M. B.; Meredith, E. L.; Hicken, E. J.; Simmons, B. L.; Glancey, R. R.; Ma, W. J. Org. Chem., 2003, 68, 8162. 9. Lee, K. C.; Moon, B. S.; Lee, J. H.; Chung, K.-H.; Katzenellenbogen, J. A.; Chi, D. Y. Bioorg. Med. Chem., 2003, 11, 3649. 10. Chen, C.-A.; Yeh, R.-H.; Lawrence, D. S. J. Am. Chem. Soc., 2002, 124, 3840. 11. Saniger, E.; Diaz-Gavilan, M.; Delgado, B.; Choquesillo, D. et al. Tetrahedron, 2004, 60, 11453. 12. Hasobe, T.; Hattori, S.; Kotani, H.; Ohkubo, K.; Hosomizu, K.; Imahori, H.; Kamat, P. V.; Fukuzumi, S. Org. Lett., 2004, 6, 3103. 13. Carato, P.; Yous, S.; Sellier, D.; Poupaert, J. H.; Lebegue, N.; Berthelot, P. Tetrahedron, 2004, 60, 10321. 14. Eichberg, M. J.; Dorta, R. L.; Grotjahn, D. B.; Lamottke, K.; Schmidt, M.; Vollhardt, K. P. C. J. Am. Chem. Soc., 2001, 123, 9324. 15. Audouin, C.; Mestdagh, N.; Lassoie, M.-A.; Houssin, R.; Henichart, J.-P. Bioorg. Med. Chem. Lett., 2001, 11, 845. 16.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无







 沪公网安备 31010602001115号
沪公网安备 31010602001115号