| 物竞编号 | 11A0 |
|---|---|
| 分子式 | C2H5Li |
| 分子量 | 36.00 |
| 标签 | Lithium Ethyl, Ethyllithium, Ethyllithium, 0.5m Solution In Benzene/ Cyclohexane (90/10), Ethyllithium 1m in benzene, 1MinBenzene, Ethyllithium solution, Ethyllithium, 1.7m solution in dibutyl ether, Ethyllithium1.7M solution in dibutyl etheracroseal§3 |
编号系统
CAS号:811-49-4
MDL号:MFCD00053747
EINECS号:212-370-2
RTECS号:暂无
BRN号:暂无
PubChem号:暂无
物性数据
1. 性状:无色或黄色有溶剂气味液体
2. 密度(g/mL,25℃):0.862
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):95
5. 沸点(ºC,常压):未确定
6. 沸点(ºC,18mmHg):172
7. 折射率(n20/D):1.49-1.493
8. 闪点(ºC):25
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(mmHg,25ºC):未确定
12. 饱和蒸气压(kPa,25ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:与水反应强烈,它溶于大多数有机溶剂中,通常在THF和乙醚中使用。
毒理学数据
暂无
生态学数据
暂无
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:3
8.表面电荷:0
9.复杂度:2.8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:2
性质与稳定性
1.避免与不相容材料火源,湿空气,空气,水,光接触。
2.与强氧化剂,水,酸类,醇类,二氧化碳,卤素,卤化物反应。
3.试剂干燥固体暴露在空气中极易着火。溶液易燃、有腐蚀性,遇水剧烈反应,因此应立即使用。低温下储藏一周,会有近一半的试剂转化为乙烷、乙烯和乙醛。
贮存方法
密封贮藏,储存在阴凉、干燥地方,冷藏,远离火源,易燃易爆区,腐蚀性领域。常用氮气保护。
合成方法
通过卤代烷与金属锂制备得到。
用途
亲核加成反应 乙基锂可以作为亲核试剂与α,β-不饱和酮进行1,2-加成 (式1)[1],有铜催化时则进行1,4-加成[2]。如果加入六甲基磷酸三酰胺 (HMPA),会提高1,4-加成的选择性,这种选择性也受溶剂配位能力的影响。在与β-苯基α,β-不饱和醛反应时,也可以在α-位进行加成 (式2)[3]。

在–78 oC条件下,乙基锂与α,β-不饱和糖酯反应,可得到高产率的1,4-加成产物。同时,非对映异构体立体选择性也非常高 (96% ee) (式3)。如果在乙基格氏试剂并有铜试剂存在的条件下,则产生另一种构型的化合物[4]。

乙基锂与乙炔、CO2一起反应,或者与异氰酸反应,可以得到共轭烯酸 (式4)[5,6],但产率比较低,所得到的烯键为顺式。

亲核取代反应 在取代的环丁烯中,苯磺酰基可以作为离去基团被乙基锂取代 (式5)[7]。

与酯作用时,乙基锂可以取代烷氧基,最终得到三级醇 (式6)[8]。

与羧酸反应时,可以形成酮 (式7)[9]。

与酰胺反应时,则使酰胺键断裂,形成酮(式8)[10,11]。

与杂原子结合 乙基锂与四配位盐{[(CH2)4P(CH2)4]+Cl–}在–60 oC下反应,将得到螺环五配位有机膦烷化合物{EtP[(CH2)4]2},但是产率较低 (式9)[12]。

安全信息
危险运输编码:UN 3399 4.3/PG 2
危险品标志: 很易燃
很易燃  有毒
有毒
危险标识:R11 R45 R46 R65 R36/38 R48/23/24/25
文献
1. Rezgui, F.; El Gaied, M. M. J. Chem. Res. (S), 1999, 576. 2. Kanai, M.; Nakagawa, Y.; Tomioka, K. Tetrahedron, 1999, 55, 3831. 3. Bremand, N.; Mangeney, P.; Normant, J. F. Tetrahedron Lett., 2001, 42, 1883. 4. Totani, K.; Asano, S.; Takao, K.; Tadano, K. Synlett, 2001, 11, 1772. 5. Smith, A. B. III; Zheng, J. Synlett, 2001, 1019. 6. Snider, B. B.; Song, F. Org. Lett., 2001, 3, 1817. 7. Knapp, K. M.; Goldfuss, B.; Knochel, P. Chem. Eur. J., 2003, 9, 5259. 8. He, Z.; Yi, C. S.; Donaldson, W. A. J. Org. Chem., 2003, 5, 1567. 9. Beier, P.; O’Hagan, D. Chem. Commun., 2002, 1680. 10. Vicario, J. L.; Rodriguez, M.; Badía, D.; Carrillo, L.; Reyes, E. Org. Lett., 2004, 6, 3171. 11. Badioli, M.; Ballini, R.; Bartolacci, M.; Giovanna Bosica, G.; Torregiani, E.; Marcantoni, E. J. Org. Chem., 2002, 67, 8938. 12. Monkowius, U.; Mitzel, N. W.; Schier, A.; Schmidbaur, H. J. Am. Chem. Soc., 2002, 124, 6126. 13.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无

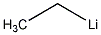



 沪公网安备 31010602001115号
沪公网安备 31010602001115号