| 物竞编号 | 0Z59 |
|---|---|
| 分子式 | C37H48N6O5S2 |
| 分子量 | 720.95 |
| 标签 | N-[(2S,3S,5R)-3-羟基-5-[[(2S)-3-甲基-2-[[甲基-[(2-异丙基-1,3-噻唑-4-基)甲基]氨基甲酰]氨基]丁酰]氨基]-1,6-二苯基-己-2-基]氨基甲酸 5-噻唑基甲基酯, 利托那韦, 瑞托那韦, 瑞托纳韦, 1,3-thiazol-5-ylmethyl n-[(2s,3s,5r)-3-hydroxy-5-[[(2s)-3-methyl-2-[[methyl-[(2-propan-2-yl-1,3-thiazol-4-yl)methyl]carbamoyl]amino]butanoyl]amino]-1,6-diphenyl-hexan-2-yl]carbamate, 1,3-THIAZOL-5-YLMETHANOL, CHEMBRDG-BB 4050354, 抗病源性微生物药 |
编号系统
CAS号:155213-67-5
MDL号:暂无
EINECS号:暂无
RTECS号:暂无
BRN号:暂无
PubChem号:暂无
物性数据
1. 性状:结晶体
2. 密度(g/mL,25℃):未确定
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):120-122
5. 沸点(ºC,常压):未确定
6. 沸点(ºC 3mm):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):不适用的
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:未确定
毒理学数据
暂无
生态学数据
暂无
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):6
2.氢键供体数量:4
3.氢键受体数量:9
4.可旋转化学键数量:18
5.互变异构体数量:16
6.拓扑分子极性表面积202
7.重原子数量:50
8.表面电荷:0
9.复杂度:1040
10.同位素原子数量:0
11.确定原子立构中心数量:4
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
暂无
贮存方法
暂无
合成方法
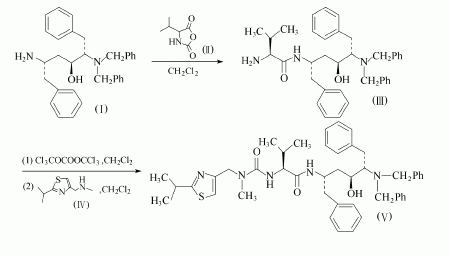
生产方法1:化合物(Ⅰ)溶于二氯甲烷,在-15℃和氮气保护下加入化合物(Ⅱ)和三乙胺的二氯甲烷溶液,搅拌2h,得到的混合液中含化合物(Ⅲ),直接用于下步反应。
往上述反应液中缓慢加入三乙胺,在-15~-13℃,将得到的混合液加到三光气的二氯甲烷溶液中,反应1.5h。缓慢加入化合物(Ⅳ)的二氯甲烷溶液,反应1h。加入水,分出有机层,用10%柠檬酸水溶液洗,浓缩。剩余物用硅胶提纯,得化合物(V),以化合物(I)计的收率为38%。
化合物(V)溶于乙酸,在钯催化下氢化。过滤,减压浓缩。剩余物溶于水,用氢氧化钠调至Ph=8。用二氯甲烷萃取,萃取液用水洗后,减压浓缩,得到化合物(Ⅵ),直接用于下步反应。
将化合物(Ⅶ)溶于乙酸乙酯,加入碳酸氢钠水溶液,反应后分层。将分出的有机层加到化合物(Ⅵ)的乙酸乙酯溶液,在60℃反应12h。浓缩,加入氨水,搅拌1h。分出有机层,分别用10%碳酸钾和氯化钠水溶液洗。减压浓缩,剩余物用硅胶提纯,得瑞托那韦,以化合物(V)计的收率为27%。

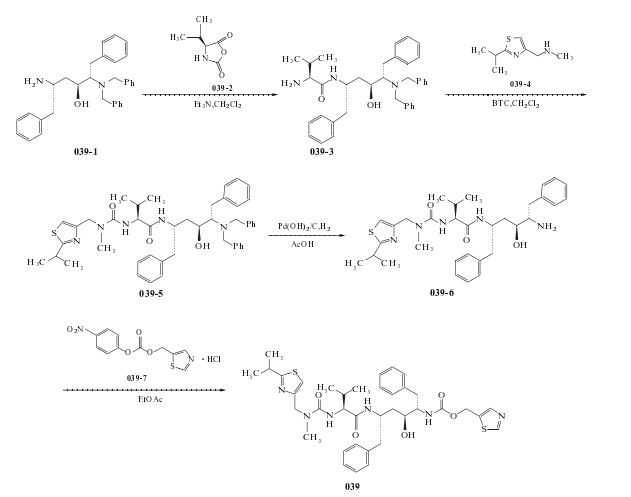
方法2:
推荐文献[8]方法.
(1).化合物039-3的制备
在反应瓶中加入胺化合物039-1(由文献[9]方法制备,它为立体异构体混合物,其比例为80:3.3:2.1:1.9)15g(32.282mmol)和二氯甲烷60ml,搅拌溶解,在N2保护下降温至-15 ºC ,搅拌加入化合物Val-NCA(039-2)6.9g(48.547mmol),紧接着滴加三乙胺[4.5ml(32.283mmol)]的二氯甲烷(48ml)溶液,于25min滴加完,滴毕,将混合物于-15~-13 ºC 搅拌反应2h(反应2h后用HPLC跟踪,分析出胺039-3含量为70.2%,原料含量4.3%).反应毕,未经进一步纯化,将该反应液直接用于下一步反应.
(2) 化合物039-5的制备
在反应瓶中加入上步制备的含胺化合物039-3的反应液一批量(32.282mmol),再慢慢加入三乙胺26ml(18.654mmol).在另一反应瓶中加入二(三氯甲基)碳酸酯(BTC;三光气)3.5g(11.794mmol)和二氯甲烷65ml,搅拌降温至-15~-13 ºC,在该温度下将上述混合液转至该反应瓶中.在同温度下将反应混合物搅拌反应1.5h[反应1.5h后用HPLC(在叔丁胺中)分析检测结果:原料胺化合物039-3含量为0.41%;中间体异氰酸酯含量为61.3%].反应达终点后,将化合物039-4 5.5g(32.282mmol)、三乙胺6.9ml(49.504mmol)溶于二氯甲烷52ml混合液于20min内,同温度下搅拌加至上述反应混合物中,加毕,继续搅拌反应1h.反应达终点后加水97ml,搅拌充分后静置分层.分取有机相,用10%柠檬酸水溶液洗涤,通过硅藻土过滤,滤液浓缩,得粗制脲化合物039-5,将粗品039-5经硅胶柱快速色谱纯化[洗脱剂:甲苯/乙酸乙酯(6:4
)].纯的039-5 9.4g,两步总收率38%.注:加入化合物039-4反应1h后,用HPLC分析:胺化合物039-3含量7%,而脲化合物039-5含量54%.)
(3)化合物039-6的制备
在加氢釜中(微型釜,配电磁搅拌或振摇搅拌)加入上步制备的化合物039-5 3.5g(4.605mmol)和乙酸31ml,搅拌加入Pd(OH)2/C催化剂5.25g,用N2置换釜内空气3次,用H2置换净N2后充H2(压力4~4.5bar)进行氢化反应,反应温度控制在78~82 ºC.搅拌氢化反应5h[反应5h后取样分析(HPLC法):039-6 52%;单苄基衍生物9.3%]后,将反应液过滤,滤液减压蒸除溶剂,得到的粗品用水35ml溶解,用NaOH调至pH8,用二氯甲烷(15ml*2)提取,分取有机层,用水10ml洗涤,有机相在减压下蒸除溶剂,得到化合物039-6 1.8g(游离碱),未经进一步纯化,直接用于下步反应(用HPLC法对其分析:游离碱胺化合物039-6 54%;单苄基衍生物6%).
(4).(5S,8S,10S,11S)-10-羟基-2-甲基乙基)-1-[2-(1-甲基乙基)-4-噻唑基]-3,6-二氧代-8,11-双(苯基甲基)-2,4,7,12-四氮杂十三-13-酸5-噻唑基甲基酯(利托那韦)(039)的合成
在反应瓶中加入化合物039-7的盐酸盐1.28g (4.03mmol)、乙酸乙酯31ml,搅拌溶解,再加入NaHCO3 370mg(4.40mmol),搅拌片刻,待固体全溶后静置分层,分取有机相备用.
在另一反应瓶中加入上步制备的化合物039-6 1.8g(3.10mmol),再加乙酸乙酯适量溶解,然后将上述制备的039-7的乙酸乙酯溶液加到化合物039-6的乙酸乙酯溶液中,搅拌升温至60 ºC ,该温度下保温反应12h.将反应液浓缩,浓缩液加入氨水,然后搅拌反应1h.出有机层,有机层用10%NaHCO3水溶液(5ml*3)洗涤,再用饱和食盐水5ml洗涤,减压蒸除溶剂,剩余物为039粗品,将其用硅胶柱快速色谱纯化[洗脱剂:乙酸乙酯],标准后处理,得039纯品900mg,两步收率为27%(以化合物039-5计).
用途
本品为抗病毒药,具有口服生物利用度高、体外氧化代谢缓慢、抗病毒活性强等特点。它对HIV-I蛋白酶具有抑制作用,其抗HIV蛋白酶作用比其母体化合物A-80987强10倍,抗纯化的重组HIV蛋白酶K1值15pmol/L.本品对已产生艾滋病毒逆转录酶药物的耐药性患者也有一定疗效.临床上本品单独使用或与其他核苷类药物配伍用于治疗晚期和非进行性艾滋病,且毒性小,耐受性好.
安全信息
危险运输编码:暂无
危险品标志:暂无
安全标识:暂无
危险标识:暂无
文献
[1] Merck Index. 13th :8321 [2] Kempf D J,et al.Proc Nat Acad Sci USA,1995,92:2484. [3] Lea A P,et al.Drugs,1996,52:541-546. [4]Nachman S A,et al.J Am Med Assoc,2000,283:492. [5] 罗明生主编,现代临床药物大典。成都:四川科学技术出版社,2001-151. [6]WO,9414436.1994. [7]US,5541206.1996. [8] WO,0121603.2001. [9] Haight A R,et al. Org Proc Rec Develop,1999,3:94-100. [10]US,5484801.1995. [11]WO,9520384.1995 [12]EP,674513.1995. [13]WO,9800393.1998. [14]WO,9911636.1999. [15]WO,9854122.1998. [16]周伟澄主编,高等药物化学选轮。北京:化学工业出版社,2006:188.
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号