| 物竞编号 | 0JX2 |
|---|---|
| 分子式 | ZnCl2 |
| 分子量 | 136.30 |
| 标签 | 锌氯粉, 盐化锌, Butter of zinc, 基因工程研究用试剂, 高纯度化合物, 缓释剂, 干电池beplay体育首页 |
编号系统
CAS号:7646-85-7
MDL号:MFCD00011295
EINECS号:231-592-0
RTECS号:ZH1400000
BRN号:暂无
PubChem号:24845378
物性数据
1. 性状:白色六方晶系粒状结晶或粉末。
2. 密度(g/mL,25/4℃):2.905
3. 熔点(ºC):283
4. 沸点(ºC,常压):732
5. 闪点(ºC): 732
6. 溶解性: 易溶于水,溶于甲醇、乙醇、甘油、丙酮、乙醚,不溶于液氨。
毒理学数据
试验方法:口服
摄入剂量:5690 mg/kg/13W-I
测试对象:啮齿动物-鼠
毒性类型:MutipleDose
毒性作用:1.大脑受影响
2.慢性数据-睾丸重量的变化
2 、
试验方法:口服
摄入剂量:910 mg/kg/26W-I
测试对象:啮齿动物-鼠
毒性类型:MutipleDose
毒性作用:诱导或改变血液或组织水平-其他酶
3 、
试验方法:口服
摄入剂量:1680年mg/kg/14D-I
测试对象:啮齿动物-鼠
毒性类型:MutipleDose
毒性作用:慢性数据-死亡
生态学数据
该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
1、 摩尔折射率:28.68
2、 摩尔体积(cm3/mol):90.8
3、 等张比容(90.2K):265.6
4、 表面张力(dyne/cm):73.2
5、 极化率(10-24cm3):11.37
计算化学数据
1、 疏水参数计算参考值(XlogP):无可用
2、 氢键供体数量:0
3、 氢键受体数量:0
4、 可旋转化学键数量:0
5、 拓扑分子极性表面积(TPSA):0
6、 重原子数量:3
7、 表面电荷:0
8、 复杂度:2.8
9、 同位素原子数量:0
10、 确定原子立构中心数量:0
11、 不确定原子立构中心数量:0
12、 确定化学键立构中心数量:0
13、 不确定化学键立构中心数量:0
14、 共价键单元数量:1
性质与稳定性
1.能自空气中吸收水分而潮解。
2.具有溶解金属氧化物和纤维素的特性。熔融氯化锌有很好的导电性能。灼热时有浓厚的白烟生成。有腐蚀性。有毒!在高温时能溶解金属氧化物,水解时生成白色氢氧化锌沉淀。
3.氯化锌非常容易潮解,必须在无水环境中保存。它对皮肤和黏膜也具有一定刺激性。
贮存方法
1.密封于2-8°C阴凉干燥环境。
2.应贮存在通风、干燥的库房内,避免露天存放。容器必须密封。防止受潮。不得与食用物品和饲料共贮混运。运输过程中应有遮盖物,要防雨淋和日晒。
3.液体用槽车装。搬运时要防止溅入眼睛或触及皮肤(其浓溶液能腐蚀皮肤,但也有杀菌作用),如接触时即用水冲去,以防皮肤腐蚀。
合成方法
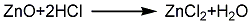
2.将纯的锌粉铺在石英舟内,并一起置于耐热玻璃管的一端。放置锌粉的一端用管式炉加热,在700℃的温度下,通入干燥的HCl气体,使其反应生成ZnCl2并升华;在耐热玻璃管的另一冷却端收集ZnCl2产品。如果反应温度超过700℃,会有一定量的锌蒸气进入升华的ZnCl2中,导致ZnCl2产品的纯度下降;此时,可将该产品在HCl气流中再次升华,以提高ZnCl2的纯度。
3.将纯净的CuCl溶解在无水乙腈中,配制成67%的溶液。用铂作阴极,纯锌板作阳极;在室温和干燥清洁的氮气保护下,对上述溶液进行电解(控制槽电压在12V以内)。电解开始时,铜首先在阴极的铂上沉积,而锌板不断地溶解;随着电解过程的进行,溶液中铜离子浓度很低时,锌会在阴极上沉积。一旦发现有灰色的锌覆盖到铜上时,电解结束。将电解后的电解液,在真空条件下,小心地加热,以蒸发掉乙腈溶剂,便可得到ZnCl2产品。
4.将锌条用5%的工业盐酸与水进行表面洗涤,置于水中,缓缓加入相对密度为1.19的盐酸(锌要过
量),搅拌,进行反应(必须严格控制加酸速度,使氢气逸出平稳):当氢气逸出速度减慢时,加热至不再产生氢气为止,静置,分离出过量锌,滤液中通氯气10~15min,然后加入少量碳酸锌,不时搅拌下加热1h,静置,过滤,滤液蒸发浓缩至原体积的1/3后,快速加热至全干(温度约230℃)。然后加入少量相对密度为1.19的盐酸,加热至400℃使盐熔化并不再跑出气体为止,冷却、粉碎,即得产品。
用途
1.用作有机合成工业的脱水剂、缩合剂及生产香兰素、兔耳草醛、消炎止痛药物、阳离子交换树脂的催化剂。可作聚丙烯腈的溶剂。染织工业用作媒染剂、丝光剂、上浆剂。纺织工业用作生产棉条桶、梭子等材料的原料(棉纤维的助溶剂),可提高纤维的黏合力。染料工业用作冰染染料显色盐的稳定剂,用于生产活性染料和阳离子染料。用作石油净化剂和活性炭的活化剂。用于浸渍木材使具有防腐性和阻燃性。用作硬纸板和布制品的阻燃剂。用于电镀。用作电焊条的焊药。冶金工业用于生产铝合金、轻金属脱酸、处理金属表面氧化层。用于晒图纸的生产。用作电池电解质。用于生产抗溶性泡沫灭火和生产氰化锌的原料。还用于医药和药的生产。
2.水处理缓蚀剂。氯化锌易溶于水,在水中水解产生不溶性胶粒,使得复合缓蚀剂呈胶状浑浊而不澄清透明,随时间延长,这些不溶性的胶粒逐渐聚集而沉淀。 为了抑制复合缓蚀剂中锌盐析出,通常加少量H2SO4、HCl、H3PO4或冰乙酸等酸性物质。
3.高浓度为腐蚀药,低浓度为收敛药,并可消毒、除臭。
4.用作分析试剂,合成阴离子交换树脂的催化剂。并用作石油净化剂和有机合成脱水剂。还用于干电池制造。
5.用于电池、钢化纸、木材防腐剂、焊药水(高温时氯化锌溶液可溶解金属氧化物),纺织工业媒染剂、上浆剂和增重剂,石油净化剂和活性炭活化剂,电镀预处理剂,药用收敛剂,农药和催化剂等,在化妆品中也用作收敛性添加剂。
安全信息
危险运输编码:UN 2331 8/PG 3
危险品标志: 腐蚀
腐蚀  危害环境
危害环境
安全标识:S26 S45 S60 S61 S36/S37/S39
文献
1. (a) Masuyama, Y.; Kinugawa, N.; Kurusu, Y. J. Org. Chem., 1987, 52, 3702. (b) Tamao, K.; Nakaji, E.; Ito. Y. J. Org. Chem., 1987, 52, 957. 2. Evans, D. A.; Nelson, J. V. J. Am. Chem. Soc., 1980, 102, 774. 3. Tamao, K.; Ishida, M.; Kumada, M . J. Org. Chem., 1983, 48, 2120. 4. Russell, C. E.; Hegedus., L. S. J. Am. Chem. Soc., 1983, 105, 943. 5. (a) King, A. O.; Okukado, N.; Negishi, E. Chem. Commun., 1977, 683. (b) King, A. O.; Negishi, E.; Villiani, Jr.; F. J.; Silveira, A. J. Org. Chem., 1978, 43, 358. 6. Negishi, E.; Okukado, N.; king, A. O.; Van Horn, D. E.; Spiegel, B. I. J. Am. Chem. Soc., 1978, 100, 2254. 7. Rao, P. S.; Venkataratnam, R. V. Tetrahedron Lett., 1991, 32, 5821. 8. Alonso, F.; Yus. M. Tetrahedron, 1991, 47, 9119. 9. Ghorai, M. K.; Das, K.; Kumar, A.; Ghosh, K. Tetrahedron Lett., 2005, 46, 4103. 10. Kim, S.; Kim, Y. J.; Ahn, K. H. Tetrahedron Lett., 1983, 24, 3369. 11. (a) Solladie, G.; Demailly, G.; Greck, C. Tetrahedron Lett., 1985, 26, 435. (b) Hanamoto, T.; Fuchikama, T. J. Org. Chem., 1990, 55, 4969. 12. (a) Tirpak, R. E.; Rathke, M. W. J. Org. Chem., 1982, 47, 5099. (b) Reetz, M. T.; Kyung, S.-H. Tetrahedron Lett., 1985, 26, 6333. 13. Prochazki, M. P.; Cartson, R. Acta. Chem. Scand., 1989, 43, 651. 14.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无





 沪公网安备 31010602001115号
沪公网安备 31010602001115号