| 物竞编号 | 03J5 |
|---|---|
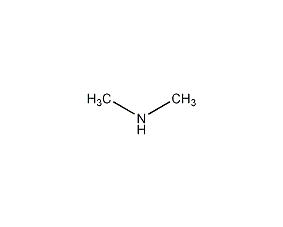
| 分子式 | C2H7N |
| 分子量 | 45 |
| 标签 | N-甲基甲胺, 脂肪族羧酸及其衍生物 |
编号系统
CAS号:124-40-3
MDL号:MFCD00008288
EINECS号:204-697-4
RTECS号:IP8750000
BRN号:605257
PubChem号:24857770
物性数据
1.性状:无色气体,高浓度的带有氨味,低浓度的有烂鱼味。[1]
2.熔点(℃):-92.2[2]
3.沸点(℃):7.0[3]
4.相对密度(水=1):0.68[4]
5.相对蒸气密度(空气=1):1.6[5]
6.饱和蒸气压(kPa):203(25℃)[6]
7.燃烧热(kJ/mol):-1743.5(液体);-1768.9(气体)[7]
8.临界温度(℃):164.5[8]
9.临界压力(MPa):5.31[9]
10.辛醇/水分配系数:-0.38[10]
11.闪点(℃):20(CC)[11]
12.引燃温度(℃):400[12]
13.爆炸上限(%):14.4[13]
14.爆炸下限(%):2.8[14]
15.溶解性:易溶于水,溶于乙醇、乙醚。[15]
16.燃点(ºC):430
17.蒸发热(KJ/mol,6.84ºC):26.50
18.生成热(KJ/mol,气体):-27.6
19.比热容(KJ/(kg·K),7.29ºC,液体,定压):3.04
20.pKa(25ºC,水):10.732
毒理学数据
1.急性毒性[16]
LD50:698mg/kg(大鼠经口);316mg/kg(小鼠经口);240mg/kg(兔经口)
LC50:8354mg/m3;4540ppm(大鼠吸入,6h);4725ppm(小鼠吸入,2h)
2.刺激性[17] 家兔经眼:50mg(5min),引起刺激。
3.亚急性与慢性毒性[18] 大鼠接触2~4mg/m3,3周,每天3h,见大脑皮质活动障碍;2~7mg/m3,7个月,每天3h,每周6d,引起可逆性机能障碍和肺、肝、肾轻度损害。
4.致突变性[19] 细胞遗传学分析:大鼠吸入50μg/m3。姐妹染色单体交换:仓鼠卵巢500μmol/L
生态学数据
1.生态毒性[20]
LC50:30~50mg/L(24h)(黑斑须雅罗鱼);120mg/L(96h)(虹鳟鱼);210mg/L(96h)(孔雀鱼)
EC50:9mg/L(96h)(绿藻);30mg/L(96h)(单细胞绿藻);26.8mg/L(15min)(发光菌,Microtox毒性测试)
2.生物降解性[21]
好氧生物降解(h):2~79
厌氧生物降解(h):8~316
3.非生物降解性[22]
空气中光氧化半衰期(h):0.892~9.2
分子结构数据
1、摩尔折射率:14.90
2、摩尔体积(cm3/mol):70.3
3、等张比容(90.2K):139.6
4、表面张力(dyne/cm):15.5
5、极化率(10-24cm3):5.91
计算化学数据
1.疏水参数计算参考值(XlogP):-0.2
2.氢键供体数量:1
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积12
7.重原子数量:3
8.表面电荷:0
9.复杂度:2.8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1、基本性质:有弱碱性,与无机酸生成易溶于水的盐类。其蒸气能与空气形成爆炸性混合物,爆炸极限2.8%-14.4%。闪点低,避免日光直射,远离火源。对铜、铜合金、铝、锡、锌等有腐蚀性。
2、化学性质具有仲胺的典型性质。例如:
① 水溶液呈碱性,与无机酸、有机酸、酸性芳香族硝基化合物生成具有一定熔点的盐。与重金属化合物形成络盐。
② 与酰氯、酸酐等发生酰基化反应,生成N-取代酰胺。与脂肪族羧酸生成的盐,经脱水后也生成N-取代酰胺。与磺酰氯、芳香族磺酰氯反应,生成相应的N-取代磺酰胺。
③ 与卤代烃、醇、酚或胺盐等烃基化试剂作用,则氮上的氢原子被烃基所取代。
④ 与氰酸、二硫化碳、腈、环氧物等能发生加成反应。
⑤ 仲胺与脂肪族或芳香族醛反应,脱水生成Schiff 碱。在碱性溶液中与甲醛反应,生成双(二烷基氨基)甲烷。或将二甲胺盐酸盐、甲醛与含有活性氢的化合物反应(Mannich反应),生成活性氢被二甲氨基甲基取代的化合物。二甲胺在碳酸钾存在下与醛反应,生成二叔胺,经蒸馏得到α,β-不饱和胺(烯胺)。
⑥ 仲胺对酸性高锰酸钾比较稳定,在碱性高锰酸钾中容易被氧化。与过硫酸、过氧化氢、有机过氧酸作用,得到胺的含氧化合物。例如,与过氧化氢作用生成二烷基羟基胺。经过氧化苯甲酸作用,生成邻苯甲酸衍生物。
⑦ 与亚硝酸反应,生成亚硝基胺。
⑧ 与Grignard试剂反应生成烃。
此外,二甲胺在420~440℃发生热裂,生成甲胺、甲烷和氢等。在紫外光照射下也能发生分解,生成甲烷等气体和高分子物质。
3.二甲胺溶液对皮肤和黏膜有强烈的刺激。长时间与高浓度蒸气接触时能引起皮肤炎、结膜炎、失明、窒息等症状。嗅觉阈浓度165mg/m3。TJ 36-79规定车间空气中最高容许浓度为10mg/m3。大鼠经口LD50为698mg/kg。兔静脉注射LD50为4000mg/kg。
4.稳定性[23] 稳定
5.禁配物[24] 强氧化剂、酸类、卤素
6.聚合危害[25] 不聚合
贮存方法
储存注意事项[26] 储存于阴凉、通风的易燃气体专用库房。远离火种、热源。库温不宜超过30℃。保持容器密封。应与氧化剂、酸类、卤素分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备。
合成方法
1.将甲醇和氨以一定比例混合,在一定温度和压力下,以活性氧化铝为催化剂,合成得一、二、三甲胺混合物,然后经热交换、冷凝、脱氨、萃取、脱水、分离,得二甲胺成品。
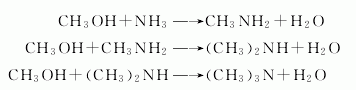
精制方法:常含有甲胺、三甲胺、氨和甲醇等杂质。可用加压蒸馏法精制。或者将二甲胺盐酸盐用乙醇反复重结晶,直至其熔点达到171℃。用氢氧化钾游离出二甲胺,再用干冰-乙醚冷却液体,固体氢氧化钾和芴酮钠干燥,可得纯净的二甲胺。其他的精制法有将二甲胺与对甲苯磺酸反应,转变成对甲苯磺酰胺。用70%乙醇重结晶,熔点达80~80.5℃后用盐酸水解使生成二甲胺盐酸盐,再按上述方法处理。
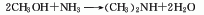
2.有弱碱性,与无机酸生成易溶于水的盐类。
用途
1.主要用作橡胶硫化促进剂、皮革去毛剂、医药(抗菌素)、农药(福美双、杀虫脒、灭草隆等除草剂)、纺织工业溶剂、染料、炸药、推进剂及二甲肼、N,N-二甲基甲酰胺等有机中间体的原料。其中二甲基甲酰胺生产消耗的二甲胺占总消耗量的44.7%,农药生产消耗占38.9%,医药等生产消耗占16.4%。也用作植物杀菌剂、除草剂、杀虫剂及酸性气体吸收剂。皮革用石灰脱毛时,可用二甲胺硫酸盐作促进剂。
2.用于有机合成及沉淀氢氧化锌等。[27]
安全信息
危险运输编码:UN 1032 2.1
危险品标志: 有毒
有毒  刺激
刺激
安全标识:S3 S16 S26 S29 S45 S36/S37/S39
危险标识:R12 R20 R34 R41 R20/22 R37/38
文献
[1~27]参考书:危险beplay体育首页 安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无





 沪公网安备 31010602001115号
沪公网安备 31010602001115号