| 物竞编号 | 0KW3 |
|---|---|
| 分子式 | BBr3 |
| 分子量 | 250.57 |
| 标签 | 溴化硼, 晶碱石, 丝光晶碱石, 碳酸钠石, 三溴硼烷, 催化剂, 溴化剂 |
编号系统
CAS号:10294-33-4
MDL号:MFCD00011312
EINECS号:233-657-9
RTECS号:ED7400000
BRN号:暂无
PubChem号:暂无
物性数据
1.性状:无色或稍带黄色的发烟液体,有强烈的刺激性臭味。[8]
2.熔点(℃):-46[9]
3.沸点(℃):90~91.2[10]
4.相对密度(水=1):2.65[11]
5.饱和蒸气压(kPa):5.33(14℃)[12]
6.辛醇/水分配系数:1.43[13]
7.溶解性:溶于四氯化碳、二氧化硫(液体)、二硫化碳。[14]
毒理学数据
1.急性毒性 暂无资料
2.刺激性 暂无资料
生态学数据
该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
1、摩尔折射率:28.67
2、摩尔体积(cm3/mol):90.0
3、等张比容(90.2K):225.5
4、表面张力(dyne/cm):39.3
5、介电常数:无可用的
6、极化率(10-24cm3):11.36
7、单一同位素质量:247.764296 Da
8、标称质量:248 Da
9、平均质量:250.523 Da
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:4
8.表面电荷:0
9.复杂度:8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.易被水和醇等分解,受热会爆炸,对人体组织有强烈刺激作用,其蒸气剧毒,腐蚀性较强,具有强吸水性,见光、遇热易分解,接触空气冒白烟。为强路易式酸,能与碱反应形成络合物和加成物。
2.在干燥空气中不变化。溶于无机酸并剧烈起泡。天然碱产于不同的盐湖沉积物中,主要产于碱湖及古代沉积矿床中,常与针碳钠钙石、水碱、泡碱、石盐、芒硝、钙芒硝、无水芒硝和石膏共生。遇空气中的湿气很容易水解。
3.稳定性[15] 稳定
4.禁配物[16] 碱类、水、醇类
5.避免接触的条件[17] 受热、潮湿空气、光照
6.聚合危害[18] 不聚合
贮存方法
储存注意事项[19] 储存于阴凉、干燥、通风良好的库房。远离火种、热源。包装必须密封,切勿受潮。应与碱类、醇类等分开存放,切忌混储。不宜久存,以免变质。储区应备有泄漏应急处理设备和合适的收容材料。
合成方法
1.直接合成法 将干燥的元素硼粉装入管式反应炉的反应管中,为使反应能充分进行,反应管内应放入一定量的填料,填料材质与管壁同。将反应管加热至850℃,另外将溴素在溴釜中也同时加热至微沸,然后通人反应管。反应生成的溴化硼液体在脱溴器中与活性炭、锌粉和铝屑共同加热回流至生成的溴化硼为无色为止,再经粗馏、精馏,制得完全无色的溴化硼成品。其反应方程式如下: 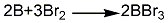
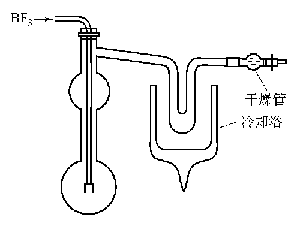 图XIII-10 三氯化硼的制备装置
图XIII-10 三氯化硼的制备装置

图XIII-11 三氯化硼的合成装置
2.用三氟化硼制备。可以使用图所示的装置。1L圆底烧瓶用一根直径约30mm、长25cm的玻璃管与500mL蒸馏烧瓶的底熔接在一起。三氟化硼的进料管通过软木塞插到蒸馏烧瓶之中,并延伸到大烧瓶的中央。500mL烧瓶是为避免大量三氯化铝与三氯化硼一起升华,起着冷凝器的作用。蒸馏烧瓶上有支管与U形管连接,U形管用干冰甲醇冷却,在U形管的出口装有干燥管。在反应烧瓶中装入67g无水三氯化铝(0.5mol)。将BF3发生装置通过硫酸洗气瓶与反应烧瓶连接起来。发生装置必须是足以发生132g(2mol)BF3的才行。BF3的流速大约为30min通过2mol的气体。在装置内通入BF3将空气逐出以后,用小火焰慢慢地加热装有三氯化铝的反应烧瓶。当温度上升时,反应立即开始,继续加热,再用两个加热器强烈加热两个烧瓶,使产物从反应混合物中分离出来,直到三氯化硼全部蒸馏出来为止。分离出生成的三氯化硼后,加热时,则三氟化铝就成为白色粉末,从烧瓶器壁上剥落下来。三氯化硼则集聚在U形管中。反应结束以后,将U形管取下密封。可用蒸馏法进行提纯。可得47g产品(80%)。
3.用KBF4制备。可用制法1的装置,以KBF4代替BF3。用133g无水三氯化铝(1mol)及62g KBF4(05mol),用油浴加热4h,缓缓地使温度从150℃上升至175℃。生成的三氯化硼用液氮冷凝,再进行蒸馏。可得30g产品(对KBF4而言,收率为52%)。
用途
1.重要的工业原料,广泛用于玻璃、化工、轻工、纺织、漂染、冶金、石油加工、医药、食品等方面。烧碱主要用于人造纤维、造纸、染料、肥皂、塑料、医药、农药等方面。小苏打主要用于食品、塑料、橡胶、医药、印染、鞣革、农业浸种等领域。
2.用作半导体的掺杂材料,有机合成的催化剂、中间体和溴化剂。是制造高纯硼及其他有机硼化合物的原料。
3.是一种用途广泛的bepaly tw ,用作有机合成的催化剂和溴化剂,也是制造高纯硼及其它有机硼化合物的原料。溴化硼可以参与促进醚键、胺键、硫醇键的断裂反应,以及丙二烯、炔烃等化合物的加成反应等。它也可以用于医药化学领域[1],天然产物化学领域[2]及新材料等领域。
溴化硼易于和C-O键反应生成烷氧基硼化物和溴代烃,水解后得到相应的醇类产物。尤其在芳甲醚的断裂反应中,溴化硼的活性明显高于其它试剂。多取代的芳环醚化合物分别和溴化硼反应可以高收率得到相应酚类物质 (式1[3],式2[4])。
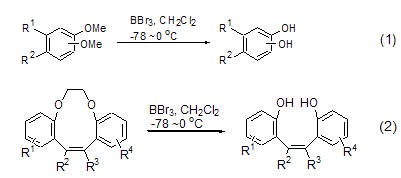
溴化硼在断裂醚键后生成的溴代烃也可以发生分子内环合反应形成环化物。如多取代芳醚化合物和溴化硼反应后生成苯并呋喃类衍生物 (式3)[5];二茂钛化合物和溴化硼反应形成钛杂环化物 (式4)[6],该反应实际是首先发生卤素交换反应,然后分子内消除反应关环而成。该反应可用于合成系列天然产物分子中的骨架结构。
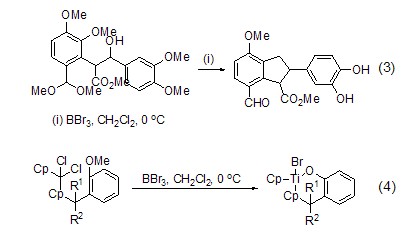
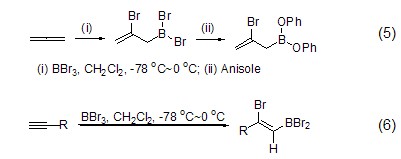
溴化硼很容易和丙二烯、炔烃等化合物进行加成反应。它和丙二烯反应得到 (2-溴烯丙基)二溴硼烷 (式5)[7],该化合物再和苯甲醚反应得到取代二苯氧基硼烷。溴化硼和炔烃通常进行顺式加成反应得到高度立体选择性的产物 (式6)[7]。
4.用于有机硼化合物和高纯硼的制取,也用作半导体的掺杂材料,有机合成的催化剂、溴化剂等。[20]
安全信息
危险运输编码:UN 2692 8/PG 1
危险品标志: 极毒
极毒  腐蚀
腐蚀
安全标识:S9 S26 S28 S45 S36/S37/S39
文献
1. Lisowski, V.; Léonce, S.; Kraus, L. B.; Sopková, O. S.; Pierré, A.; Atassi, G.; Caignard, D.; Renard, P.; Rault, S. J. Med. Chem., 2004, 47, 1448. 2. Brimble, M. A.; Brenstrum, T. J. J. Chem. Soc., Perkin Trans 1, 2001, 1624. 3. Barluenga, J.; Aznar, F.; Palomero, M. A. J. Org. Chem., 2003, 68, 537. 4. Mayekar, N. V.; Chattopadhyay, S.; Nayak, S. K. Synthesis, 2003, 2041. 5. Detterbeck, R.; Hesse, M. Helv. Chim. Acta., 2003, 86, 343. 6. Qian, Y.; Huang, J.; Ding, K.; Zhang, Y.; Huang, Q.; Chen, X.; Chan, A.; Wong, W. J. Organomet. Chem., 2002, 645, 59. 7. Hara, S.; Suzuki, A. Tetrahedron Lett., 1991, 32, 6749. [1~7]参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7 [8~20]参考书:危险beplay体育首页 安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号