| 物竞编号 | 0RL1 |
|---|---|
| 分子式 | SmI2 |
| 分子量 | 404.17 |
| 标签 | 二碘化钐(II), Samarium(II) diiodide |
编号系统
CAS号:32248-43-4
MDL号:MFCD00058873
EINECS号:203-726-8
RTECS号:暂无
BRN号:暂无
PubChem号:24865638
物性数据
1.性状:蓝色-深蓝色液体,具有特殊气味。
2.密度(g/mL,25℃):0.922
3.相对蒸汽密度(g/mL,空气=1):未确定
4.熔点(ºC):527
5.沸点(ºC,常压):1580
6.沸点(ºC,KPa):未确定
7.折射率:未确定
8.闪点(ºC):-18.9
9.比旋光度(º):未确定
10.自燃点或引燃温度(ºC):未确定
11.蒸气压(Pa,20ºC):未确定
12.饱和蒸气压(KPa,25ºC):未确定
13.燃烧热(KJ/mol):未确定
14.临界温度(ºC):未确定
15.临界压力(KPa):未确定
16.油水(辛醇/水)分配系数的对数值:未确定
17.爆炸上限(%,V/V):未确定
18.爆炸下限(%,V/V):未确定
19.溶解性:在极性有机溶剂中有一定的溶解度,通常在THF,HMPA中使用。
毒理学数据
急性毒性:
Oral:LD50:2300mg/kg(gpg)
LD50:1650mg/kg(rat)
Inhalative:LC50/3H:21000ppm/3H(rat)
主要的刺激性影响:
在皮肤上面:刺激皮肤和粘膜。
在眼睛上面:刺激的影响
致敏作用:没有已知的敏化作用。
生态学数据
总括注解
水危害级别1(德国规例)(通过名单进行自我评估)该物质对水有稍微危害的。
不要让未稀释或大量的产品接触地下水、水道或污水系统。
若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1、 疏水参数计算参考值(XlogP):
2、 氢键供体数量:0
3、 氢键受体数量:0
4、 可旋转化学键数量:0
5、 互变异构体数量:
6、 拓扑分子极性表面积(TPSA):0
7、 重原子数量:3
8、 表面电荷:0
9、 复杂度:2.8
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:1
性质与稳定性
1.如果遵照规格使用和储存则不会分解,未有已知危险反应。
2.遇水分解生成碱式碘化钐和氢气。有强还原性。
3.具有较强的吸湿性,对氧气特别敏感,需要在惰性气体保护下制备和使用。
贮存方法
贮存:一般保存于约0.1mol/L的四氢呋喃溶液中。
合成方法
按照标准的实验步骤从金属钐和碘在THF中来制备[1]。
用途
碘化钐(SmI2)是有机合成中一个具有广泛用途的试剂。它参与的主要反应包括:自由基环化反应;羰基-烯烃偶联反应;频哪偶联反应;羟醛缩合反应;Barbier反应;Reformatsky反应等。已经有多篇论文对它们的性质和应用进行了详细的综述[2]。
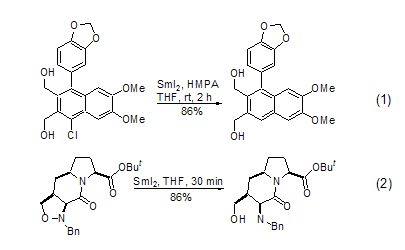
SmI2最基本的反应是它的还原反应。在HMPA作为共溶剂的情况下,它可以方便地除去底物分子中的卤原子 (式1)[3]。在可见光照射的情况下,不使用HMPA 也可以得到同样的结果[4]。杂原子键,例如N-N[5]或者N-O[6]键,在SmI2的作用下能够发生选择性断裂,这种性质在多官能团复杂化合物的合成中特别有用 (式2)。
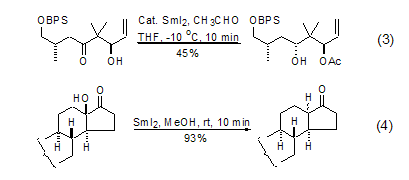
SmI2的特征反应之一是在一分子醛的存在下,1,3-羟基酮在低温下数分钟内被还原成为1,3-二羟基化合物的单酯衍生物。反应的机理可能是通过一个环状过渡态进行的,所以反应中新形成的羟基保持高度的立体选择性 (式3)[7,8]。α-羟基酮在SmI2的作用下,一分钟之内可以将羟基除去生成相应的酮 (式4)[9~11]。
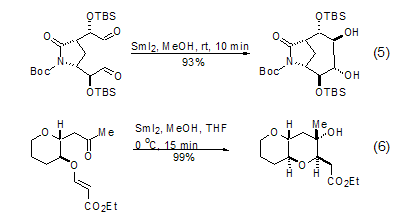
二醛在SmI2的作用下发生频呐醇偶联反应,生成大环化合物。该反应不仅反应条件简单,而且给出比较满意的产率 (式5)[12,13]。SmI2参与的最有价值的反应是羰基-烯烃偶联反应。使用带有拉电子基团的缺电子烯烃有助于提高反应的收率 (式6)[14,15]。
安全信息
危险运输编码:UN 2056 3/PG 2
危险品标志: 易燃
易燃  刺激
刺激
文献
1. Molander, G. A.; Wolfe, C. N. J. Org. Chem., 1998, 63, 9031. 2. (1) Molander, G. A. Chem. Rev., 1992, 92, 29. (2) Molander, G. A.; Harris, C. R. Chem. Rev., 1996, 96, 307. 3. Nishii, Y.; Yoshida, T.; Asano, H.; Wakasugi, K.; Morita, J.-i.; Aso, Y.; Yoshida, E.; Motoyoshiya, J.; Aoyama, H.; Tanabe, Y. J. Org. Chem., 2005, 70, 2667. 4. Sumino, Y.; Harato, N.; Tomisaka, Y.; Ogawa, A. Tetrahedron, 2003, 59, 10499. 5. Friestad, G. K.; Korapala, C. S.; Ding, H. J. Org. Chem., 2006, 71, 281. 6. Manzoni, L.; Arosio, D.; Belvisi, L.; Bracci, A.; Colombo, M.; Invernizzi, D.; Scolastico, C. J. Org. Chem., 2005, 70, 4124. 7. Evans, D. A.; Hoveyda, A. H. J. Am. Chem. Soc., 1990, 112, 6447. 8. Blakemore, P. R.; Browder, C. C.; Hong, J.; Lincoln, C. M.; Nagornyy, P. A.; Robarge, L. A.; Wardrop, D. J.; White, J. D. J. Org. Chem., 2005, 70, 5449. 9. Hartung, R.; Paquette, L. A. J. Org. Chem., 2005, 70, 1597. 10. aquette, L. A.; Seekamp, C. K.; Kahane, A. L.; Hilmey, D. G.; Gallucci, J. J. Org. Chem., 2004, 69, 7442. 11. Jiang, X.; Wang, C.; Hu, Y.; Hu, H. J. Org. Chem., 2000, 65, 3555. 12. Curti, C.; Zanardi, F.; Battistini, L.; Sartori, A.; Rassu, G.; Auzzas, L.; Roggio, A.; Pinna, L.; Casiraghi, G. J. Org. Chem., 2006, 71, 225. 13. Ueda, T.; Kanomata, N.; Machida, H. Org. Lett., 2005, 7, 2365. 14. Sato, K.; Sasaki, M. Org. Lett., 2005, 7, 2441. 15. Clarke, P. A.; Cridland, A. P. Org. Lett., 2005, 7, 4221. 16.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号