| 物竞编号 | 0KNA |
|---|---|
| 分子式 | SnBr2 |
| 分子量 | 278.52 |
| 标签 | 二溴化锡 |
编号系统
CAS号:10031-24-0
MDL号:MFCD00011239
EINECS号:233-087-0
RTECS号:暂无
BRN号:暂无
PubChem号:暂无
物性数据
1. 性状:黄色晶体。
2. 密度(g/mL,20℃):5.12
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):232
5. 沸点(ºC,常压):620
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,20ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:溶于水。
毒理学数据
生态学数据
通常对水体是稍微有害的,不要将未稀释或大量产品接触地下水,水道或污水系统,未经政府许可勿将材料排入周围环境。
分子结构数据
1、摩尔折射率:无可用的
2、摩尔体积(cm3/mol):无可用的
3、等张比容(90.2K):无可用的
4、表面张力(dyne/cm):无可用的
5、介电常数:无可用的
6、极化率(10-24cm3):无可用的
7、单一同位素质量:277.738859 Da
8、标称质量:278 Da
9、平均质量:278.518 Da
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:0
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:3
8.表面电荷:0
9.复杂度:2.8
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
可溶于水、乙醇、乙醚、丙酮,其稀水溶液会发生水解。
贮存方法
暂无
合成方法
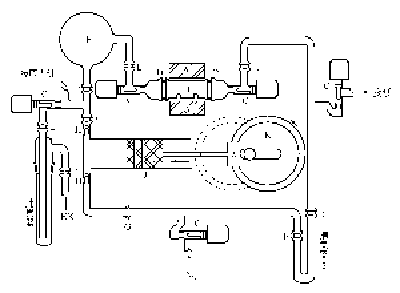
图XIV-23 制备溴化亚锡的循环系统
1.烧瓶中加入粉末状锡和浓氢溴酸,在砂浴上加热至氢气发生结束,过滤分离除去未反应的锡。将滤液与少量的锡箔共同在水浴上加热浓缩至少量的盐析出。冷却后析出黄色针状结晶,迅速用玻璃砂芯漏斗进行抽滤,结晶放在素瓷板上置于盛有浓硫酸的真空干燥器中干燥。待结晶还湿润时,将其移至烧瓶中,在氮气氛下直接用火加热,加热逐渐由弱至强,最初产生水,接着溴化氢加合物分解产生溴化氢。当停止产生气体时,形成SnBr2的透明熔融体,在氮气流中冷却。产物可用石英蒸馏瓶在氮气流中蒸馏精制。
2.反应原理同制法1。设计一个循环装置,让适量的HBr气体通过熔化的锡上方生成SnBr2。SnBr2受热升华,凝结在较冷的反应管两端。而不断暴露出的锡表面继续与HBr反应,这是一个半自动化的合成方法。
图中装置均用硼硅酸耐热玻璃制作,所有的接口和活塞都带O形密封圈,材质为聚四氟乙烯。活塞大小与直径25mm气缸相配。用带有蓝宝石珠的毛玻璃止逆阀作气阀。活塞涂黄油润滑。驱动活塞的电机用110V交流电,3600r/min,换低速挡600∶1。活塞通过偏心轮连接推杆,冲程为2.54cm。
图制备溴化亚锡的循环系统
A—管式炉;B—反应管;C—聚四氟乙烯塞;D—15mm O形接口;
E—9mm O形接口;F—平衡容器;G—9mm球窝连接器;
H—止逆阀;I—玻璃气缸;J—聚四氟乙烯喷枪;K—偏心轮
将市售的锡粒在石英烧瓶中加热熔化后倾倒入一支大玻璃试管中,除去表面粗糙的氧化产物。冷却后取出锡,并将锡切割成如同反应器大小。反应器(B)是可拆卸的,将锡放入其中的玻璃凹槽间,大致10g,将系统连接好,开泵抽真空,在280℃下保持1h。捕集器1保持在-78℃,让HBr气体充满系统达101325kPa。为了除去不可冷凝的气体,HBr气在-196℃的捕集器2中冷凝,系统再被抽真空。然后体系关闭,将捕集器2升温至25℃,活塞开始工作,HBr气体逐渐被H2取代,约12h后被耗尽,停活塞,捕集器2再冷却到-196℃,剩余反应物又冷凝在此,可卸下捕集器2,H2用泵抽走。关掉往复泵,体系在真空下运转,反应器在280℃保温1h,产品升华,直至锡表面不再有SnBr2产品,然后冷却系统,关闭聚四氟乙烯塞,隔离反应部分,卸下反应管,将产品回收到干燥器中。
HBr的用量由系统的体积和压力估算出,反应中锡是过量的。一次实验中得到4.0gSnBr2,产率达70%。
用途
暂无
安全信息
危险运输编码:暂无
危险品标志:暂无
安全标识:暂无
危险标识:暂无
文献
暂无
备注
暂无

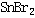



 沪公网安备 31010602001115号
沪公网安备 31010602001115号