| 物竞编号 | 0S7V |
|---|---|
| 分子式 | C9H9NO2S |
| 分子量 | 195.24 |
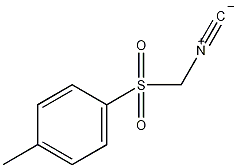
| 标签 | 对甲苯磺酰甲基胩, (p-Tolylsulfonyl)methyl isocyanide, TosMIC, Tosylmethyl isocyanide |
编号系统
CAS号:36635-61-7
MDL号:MFCD00000005
EINECS号:253-140-1
RTECS号:暂无
BRN号:3592382
PubChem号:24889279
物性数据
1. 性状:白色固体
2. 密度(g/mL,20℃):未确定
3. 相对蒸汽密度(g/mL,空气=1): 未确定
4. 熔点(ºC):113-115
5. 沸点(ºC,常压): 未确定
6. 沸点(ºC,0.9mm hg):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC): 未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC): 未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:能够溶于大多数有机溶剂,通常在醚类溶剂中使用,例如THF。
毒理学数据
暂无
生态学数据
对水是稍微有危害的不要让未稀释或大量的产品接触地下水、水道或者污水系统,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):1.3
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:2
5.互变异构体数量:无
6.拓扑分子极性表面积46.9
7.重原子数量:13
8.表面电荷:0
9.复杂度:298
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.常规情况下不会分解,没有危险反应。
2.对空气和湿气相对比较稳定。
贮存方法
密封、阴凉、干燥、通风保存
合成方法
1.通过N-(对甲苯磺酰甲基)甲酰胺脱水来制备[1]。
2.一对甲苯磺酞甲共甲酰胺的制备在装有机械搅拌器、冷凝器和温度计的3升三颈园底烧版中,放入267克(1.5摩尔)对甲苯亚磺酸钠、750毫升水、350毫升(378克)34-37%甲醛溶液(约4.4摩尔)、600毫升(680克,15摩尔)甲酰胺和200毫升(244克,5.3摩尔)97%甲酸,在90℃加热并搅拌反应混合物。受热时对甲苯亚磺酸钠A解。将清亮溶液保持90一95℃2小时。在冰盐浴中继续搅拌下冷却至室温,然后在一20℃冷藏箱中进一步冷却过夜。吸滤,收集白色固体。在烧杯中用3份250毫升冰水在搅拌下充分洗涤。产物在五氧化二磷上70℃减压于燥得134一150克(42一47%粗N一(对甲苯磺酞甲基)甲酰铵。
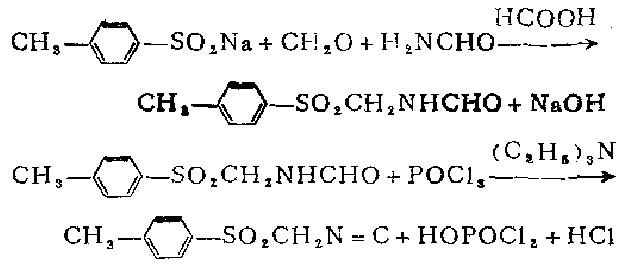
3.对甲苯磺c甲基异精的制备在装有机械搅拌器、温度计、250毫升滴液漏斗和干JF.管灼3升四颈园底烧瓶中,盛107克(0.50摩尔)粗N-对甲苯磺酞甲基)甲酞胺、250毫升}.一二甲氧基乙烷、100毫升无水乙醚和肠o毫升(255克,2.5摩尔)三乙胺。将搅拌,知的悬浮液在冰一盐浴中冷却至一5℃,然后从滴液漏斗中以保持深度在一5一0℃的速度加入50毫升〔84克,0.55摩尔)三氯氧磷i齐牙几60毫升1.2一二甲J氧基乙烷的溶液。在此反应过程中,N一(对甲苯磺酞甲基)甲酞胺渐渐浓解,而三乙胺的盐则沉淀出来。反应近于完成时,白色悬浮液慢慢变成棕色。在。℃再搅拌3。分钟。在继续搅拌下加入1.5升冰水。在产物开始析出成细小棕色结晶1司体前,固体物质溶解而成清亮的暗棕色溶液。在0℃搅拌}J分钟后,吸滤出沉淀,用250毫升冷水洗涤。湿产物溶于400毫升热苯(40一60℃),用分液漏斗分出水层,暗棕色的苯
i容液.明无水硫酸镁干},h除去硫酸镁后,加2克活性炭。加热至约60℃5钟,过滤。在旋荡下加1升石油醚(沸点40一80℃)于滤液中。30分钟.后,吸滤出沉淀,在真空干爆器巾干燥。得(76-84%)粗对甲苹磺醚异腈。
用途
1.制备腈。合成杂环如唑,嘧啶,吡咯。噻唑。三唑等。由酮制a一羟醛。合成酮和1,2一二酮等。
2.对甲苯磺酰甲基异氰 (TosMIC) 是有机化学官能团转换反应中最有用的多功能试剂和合成子之一。TosMIC在杂环合成中可以用来方便地制备咪唑、噻唑、恶唑、三氮唑、吲哚、吡咯等。TosMIC参与的增加一个碳原子的还原氰基化反应和二烷基化反应具有独到之处。最近刚刚出版的一篇论文对TosMIC化学进行了详细的综述[1]。
TosMIC与酮生成腈的还原氰基化反应是该试剂最特征的反应之一。反应的机理是TosMIC在碱的存在下生成碳负离子与酮羰基发生亲核加成反应,然后失去磺酰基和甲酰基生成腈[2]。该反应需要使用过量的碱,常用的碱为t-BuOK。反应一般在室温下数小时内完成,产率中等到较高水平 (式1,式2)[3,4]。TosMIC与甾体17-酮反应时,生成两种异构体的混合产物 (式3)[5]。

TosMIC与卤代烃发生烷基化反应,生成多一节碳的酮[6,7]。分子间的烷基化反应生成对称或者不对称的链状酮,分子内的烷基化反应生成相应的环状酮 (式4,式5)[6,7]。

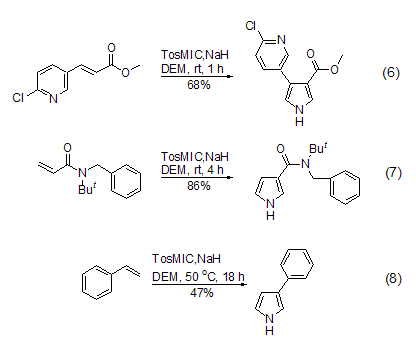
TosMIC与α,β-不饱和羰基化合物反应生成吡咯环的反应一般给出较好的产率,羰基或者其它拉电子基团的存在对反应活性的影响非常大 (式6,式7)[8,9]。最近有人报道简单的芳基乙烯就可以与TosMIC发生形成吡咯环的反应 (式8)[10]。
安全信息
危险运输编码:UN 2811 6.1/PG 3
危险品标志: 有毒
有毒
安全标识:暂无
危险标识:暂无
文献
1. 综述文献见:van Leusen, D.; van Leusen, A. M. Org. React., 2003, 57, 417. 2. Oldenziel, O. H.; van Leusen, D.; van Leusen, A. M. J. Org. Chem., 1977, 42, 3114. 3. Peterlin-Masic, L.; Jurca, A.; Marinko, P.; Jancar, A.; Kikelj, D. Tetrahedron, 2002, 58, 1557. 4. Boyer, F-D.; Hanna, I.; Ricard, L. Org. Lett., 2004, 6, 1817. 5. Hu, Y.; Zorumski, C. F.; Covey, D. F. J. Med. Chem., 1993, 36, 3956. 6. Yasutake, M.; Araki, K.; Zhou, M.; Nogita, R.; Shinmyozu, T. Eur. J. Org. Chem., 2003, 1343. 7. Yang, J.; Duan, C.; Pop, E.; Geoffroy, O. J.; Zhang, L.; Huang, T.; Denisenko, S.; McCosar, B. H.; Oniciu, D. C.; Bisgaier, C. L. J. Med. Chem., 2004, 47, 6082. 8. Pavri, N. P.; Trudell, M. L. J. Org. Chem., 1997, 62, 2649. 9. Smith, N. D.; Huang, D.; Cosford, N. D. P. Org. Lett., 2002, 4, 3537. 10. Clayden, J.; Turnbull, R.; Pinto, I. Org. Lett., 2004, 6, 609. 11.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号