| 物竞编号 | 0NCJ |
|---|---|
| 分子式 | CeN8H8O6N18 |
| 分子量 | 548.22 |
| 标签 | 硝酸铈铵, 硝酸铵铈, 硝酸銨鈰, 硝酸鈰銨, Ammonium cerium(IV) nitrate, Ammonium hexanitro cerate, CAN, 显色剂,氧化剂,催化剂; |
编号系统
CAS号:16774-21-3
MDL号:MFCD00151121
EINECS号:240-827-6
RTECS号:暂无
BRN号:暂无
PubChem号:24853335
物性数据
1. 性状:橙红色单斜细粒结晶。在空气中易潮解。
2. 密度(g/mL,25/4℃): 1.10 g/mL at 20 °C
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):107-108 °C
5. 沸点(ºC,常压):未确定
6. 沸点(ºC,5.2kPa):未确定
7. 折射率:未确定
8. 闪点(ºC):未确定
9. 比旋光度(º):未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值:未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性:易溶于水和乙醇,几乎不溶于浓硝酸。也溶于醇类、硝酸等质子性溶剂,在乙腈中有一定溶解性,不溶于二氯甲烷、三氯甲烷和四氯化碳。
毒理学数据
暂无
生态学数据
通常对水体是稍微有害的,不要将未稀释或大量产品接触地下水,水道或污水系统,未经政府许可勿将材料排入周围环境。
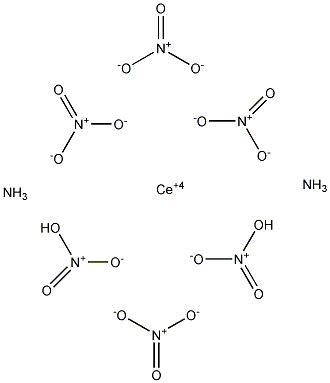
分子结构数据
暂无
计算化学数据
1、 疏水参数计算参考值(XlogP):
2、 氢键供体数量:6
3、 氢键受体数量:18
4、 可旋转化学键数量: 0
5、 互变异构体数量:
6、 拓扑分子极性表面积(TPSA):380
7、 重原子数量:25
8、 表面电荷:0
9、 复杂度:24.8
10、 同位素原子数量:0
11、 确定原子立构中心数量:0
12、 不确定原子立构中心数量:0
13、 确定化学键立构中心数量:0
14、 不确定化学键立构中心数量:0
15、 共价键单元数量:7
性质与稳定性
具有低毒性。
贮存方法
本品应密封于阴凉干燥处保存。
合成方法
1. 将85g稀土氟化物 ( 含28%二氧化铈、37.7%其他稀土金属氧化物及4.5%的氧化钙)和 50ml水共置于250ml的铂皿或铅皿中,在砂浴上加热,搅拌下缓缓加入密度为1.84的150ml硫酸,进行反应:

因有HF逸出而起泡,连续加热10~15h,不时搅拌一下,直到逸出SO3气体为止。冷却后将混合物移入装有750ml热水的容器中,用250ml水洗涤沉淀物,再将混合物搅拌2h,静置,过滤。将上述操作重复进行三次而得到的水溶液,加热至70-80℃,加入含有600g氢氧化钠的1LK水溶液,至石蕊呈强碱性,沉淀由白色转为灰色:
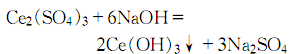
静置,澄清,沉淀用热水倾析洗涤至犛 犗 2- 4 离子合格。将此沉淀移入大烧杯,加入2~3L含有50g氢氧化钠的溶液,并强烈搅拌,同时在20~25℃通入氯气 ( 约100L) ,以氧化Ce3+:
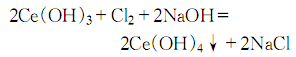
其他铈元素以氯化物形式进入溶液,将空气通入溶液中,并缓缓加热2~3h,以除去多余氯,直至无氯气味。静置,澄清后,分去液层,沉淀用水倾析洗涤至不存在 Cl-离子。抽滤后,用密度为1.40的分析纯硝酸250ml溶解沉淀 物,加 热 蒸 发 成 糖 浆 状 ( 约300ml ) ,再加入180~200g析纯的硝酸铵结晶体,并重新蒸发到生成糊状结晶体:
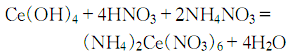
冷却结晶,结晶抽滤,用密度为1.40的硝酸洗涤二次,每次10~20ml,再溶解于200ml水中,加入25ml硝酸,过滤,将滤液蒸发到糊状,冷却结晶,过滤后,用硝酸洗涤二次,将母液与洗涤水一起蒸发至糊状,冷却结晶,将三次的结晶物 ( 共150~170g)再重结晶一次,于75~85℃干燥,制得的试剂含硝酸铈铵99.5%。
用途
1.用于微量银离子的测定。氧化还原滴定剂。烯烃聚合催化剂。
2.用作分析试剂,常用于配制氧化还原滴定标准溶液,用作薄层色谱法检测多元醇的显色剂,制备磷酸盐敏感的膜电极组成物的原料物质以及用作电位滴定法测定各种胺类的试剂。还可作氧化剂,烯烃聚合催化剂。
3.硝酸铈铵CAN是一个强氧化剂,在酸性条件下氧化性更强,仅次于F2、XeO3、Ag2+、O3、HN3。在水溶液和其它质子溶剂中,CAN是一个单电子氧化剂,从颜色的变化(从橙色到淡黄色)可判断CAN的消耗情况。由于在有机溶剂中溶解度的局限性,因此CAN参与的反应大多在混合溶剂如水/乙腈中进行。在其它氧化剂如溴酸钠、叔丁基过氧化氢和氧气等的存在下,可实现Ce4+的循环使用,从而实现催化反应。此外,CAN还是一个有效的硝化试剂。
CAN对醇、酚、醚等含氧化合物具有氧化活性,其中对二级醇具有特异氧化性。如将苄醇氧化为对应的醛酮 (式1)[2],甚至对硝基苄醇也能被CAN/O2催化氧化体系氧化为对硝基苄酮。此外,对于特殊二级醇如4-烯醇或5-烯醇等,还可以得到环醚化合物 (式2)[3]。
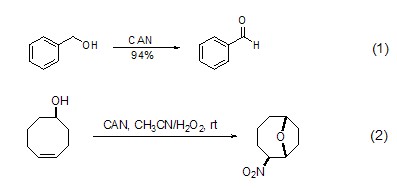
对于邻苯二酚、对苯二酚以及它们的甲基醚化合物,在CAN作用下能够被氧化为醌。如邻苯二酚转换为邻苯醌 (式3)[4]、对苯二酚在CAN和超声波作用下快速转换为对苯醌 (式4)[5],以及芳基醚转换为对苯醌的反应。

对于环氧化合物的氧化反应还可以得到二羰基化合物 (式5)[6]。此外,CAN对特定结构的羰基化合物也具有氧化活性,如将多环笼酮氧化为内酯的反应 (式6)[7]。
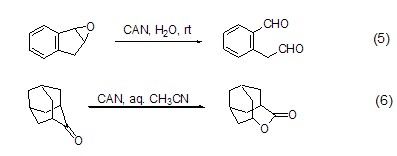
作为单电子氧化剂,CAN还能实现分子间或分子内的碳-碳键形成反应。如1,3-二羰基化合物与苯乙烯系统在CAN作用下的氧化加成反应 (式7)[8],或者苯胺自身的二聚反应 (式8)[9]。
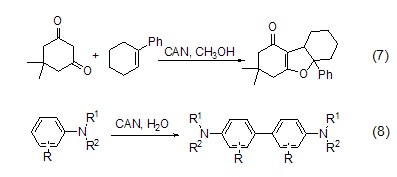
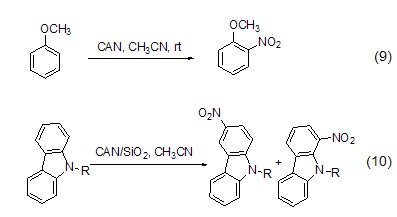
除了氧化反应外,CAN还是一个有效的硝化试剂,特别是对芳环系统的硝化。如在乙腈中CAN与苯甲醚作用得到邻位硝化产物 (式9)[10]。但是由于CAN的强氧化性,往往使得芳环系统发生多硝化反应,甚至生成难以分离的聚合物。研究发现,将CAN吸附在硅胶上可降低其氧化性,从而减少多硝基产物的生成。如在乙腈中,以硅胶为载体,用CAN对咔唑和9-烷基咔唑进行硝化,产率可提高到70%~80% (式10)[11]。
安全信息
危险运输编码:UN 1477 5.1/PG 2
危险品标志:暂无
安全标识:暂无
危险标识:暂无
文献
1. (a) Nair, V.; Balagopal, L.; Rajan, R.; Mathew, J. Acc. Chem. Res. 2004, 37, 21. (b) Nair, V.; Mathew, J.; Prabhakaran, J. Chem. Soc. Rev., 1997, 26, 127. 2. (a) Trahanovsky, W. S.; Young, L. B.; Brown, G. L. J. Org. Chem., 1967, 32, 3865. (b) Fisher, T. H.; Dershem, S. M.; Schultz, T. P. J. Org. Chem., 1988, 53, 1504. 3. (a) Kim, H. J.; Schlecht, M. F. Tetrahedron Lett., 1988, 29, 1771. (b) Wilson, S. R.; Augelli-Szafran, C. E. Tetrahedron, 1988, 44, 3983. 4. Francesco, C.; Ettore, N. Synth. Commun., 1986, 16, 968. 5. Morey, J.; Saa, J. M. Tetrahedron, 1993, 49, 105. 6. Roy, S. C.; Adhikari, S. Indian. J. Chem., Sect. B., 1992, 31B, 459. 7. (a) Hintz, H. L.; Johnson, D. C. J. Org. Chem., 1967, 32, 556. (b) Trahanovsky, W. S.; Young, L. H.; Bierman, M. H. J. Org. Chem., 1969, 34, 869. 8. Nair, V.; Balagopal, L.; Rajan, R.; Mathew, J. Acc. Chem. Res., 2004, 37, 21. 9. Xi, C.; Jiang, Y.; Yang, X. Tetrahedron Lett., 2005, 46, 3909. 10. Dhanalekshmi, S.; Balasubramanian, K. K.; Venkatachalam, C. S. Tetrahedron, 1994, 50, 6387. 11. Manas, C.; Archana, B. Synth. Commun., 1994, 24, 3. 12.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无




 沪公网安备 31010602001115号
沪公网安备 31010602001115号