| 物竞编号 | 0K6M |
|---|---|
| 分子式 | KF |
| 分子量 | 58.10 |
| 标签 | 氟化钾,无水, 无水氟化钾, 氟化鉀, 氟化钾, Potassium fluoride, Potassium fluoride on celite(R), Fluorure de potassium, fluoruredepotassium, KF, Potassium fluoride (KF), Potassium fluorure, 杀虫剂, 氟化剂, 催化剂, 吸收剂 |
编号系统
CAS号:7789-23-3
MDL号:MFCD00011398
EINECS号:232-151-5
RTECS号:TT0700000
BRN号:暂无
PubChem号:24868456
物性数据
1.性状:无色立方结晶,易潮解。[7]
2.熔点(℃):858[8]
3.沸点(℃):1505[9]
4.相对密度(水=1):2.48[10]
5.饱和蒸气压(kPa):0.133Pa(885℃)[11]
6.溶解性:溶于水、氢氟酸、液氨,不溶于乙醇。[12]
毒理学数据
1.急性毒性[13] LD50:245mg/kg(大鼠经口)
2.刺激性 暂无资料
生态学数据
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
分子结构数据
1、摩尔折射率:无可用的
2、摩尔体积(cm3/mol):无可用的
3、等张比容(90.2K):无可用的
4、表面张力(dyne/cm):无可用的
5、介电常数:无可用的
6、极化率:无可用的
7、单一同位素质量:57.96211 Da
8、标称质量:58 Da
9、平均质量:58.0967 Da
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积0
7.重原子数量:2
8.表面电荷:0
9.复杂度:2
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:2
性质与稳定性
1.易溶于水,能溶于氢氟酸和液氨,微溶于醇及丙酮。水溶液呈碱性,能腐蚀玻璃及瓷器。加热至升华温度时才少许分解,但熔融氟化钾的活性较大,能腐蚀耐火物质。与过氧化氢可形成加成物KF·H2O2。水合物有两种:KF·2H2O和KF·4H2O。低于40.2℃时,水溶液中可结晶得到二水物(KF·2H2O),系单斜晶体,41℃时可自溶于结晶水中。有毒。
2.KF作为制备各种有机氟化物的氟化剂被广泛使用。
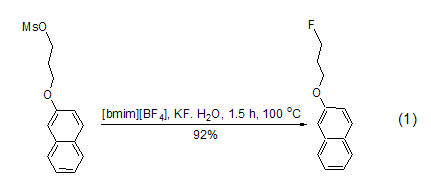
最近提出一种在离子液体-水体系中进行氟化的新方法。在[bmim][BF4]存在下,烷基卤代物和烷基甲磺酰基取代物用KF处理得到氟化产物 (式1)[1]。该方法能够大大提高氟化物的反应活性和选择性。
KF存在下,六氟代烷基-或六氟代苯基三甲基硅烷与醛、酮、酰基氟化物反应得到氟代醇 (式2)[2]。磺酰基氟化物作底物则以很好的产率得到砜。这些反应通常在偶极溶剂中进行,如MeCN 和PhCN等。
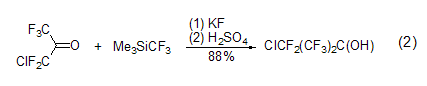
KF可促进有机氟代硅烷与碘代芳烃在钯催化下的羰基偶联反应 (式3)[3]。
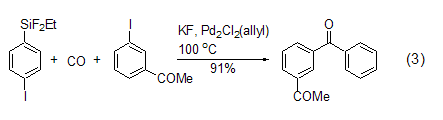
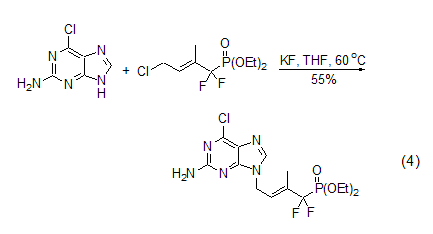
DMSO中的KF是一种很好的脱HCl试剂。卤代烯或卤代烷在KF作用下能脱HCl生成炔烃、丙二烯、链烯及共轭二烯等。反应体系中有冠醚存在的条件下有利于消除反应,尤其在MeCN作为溶剂的时候。KF还可以促进醇、酚、硫醇、胺与卤代烷的烷烃化反应。这种方法已被用于冠醚的合成。杂环也可以被烯丙基卤代物烷基化 (式4)[4]。KF作催化剂,苯酚可以与活化的芳基氟发生芳基化反应。
在羧酸和卤代烷转化成酯的反应中加入KF能够大大提高反应产率 (式5)[5]。这个反应用反应物酸作为溶剂;当起始原料酸为固体时,则可以用DMF为溶剂。反应活性最好的底物是碘代烷。
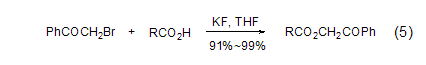
KF还能用于促进Fischer烷氧基卡宾复合物的氧化。在KF或Bu4NF作用下,Fischer烷氧基卡宾复合物的金属部分可以被氧化除去,形成相应的酯类似物。该方法简单且低成本 (式6)[6]。

3.稳定性[14] 稳定
4.禁配物[15] 强酸
5.聚合危害[16] 不聚合
贮存方法
储存注意事项[17] 储存于阴凉、通风的库房。远离火种、热源。包装密封。应与酸类、食用beplay体育首页 分开存放。切忌混储。储区应备有合适的材料收容泄漏物。
合成方法
1.中和法在中和池内用等量水溶解固体氢氧化钾,然后通入无水氢氟酸(或40%氢氟酸)进行反应,至Ph=7~8时,停止通人无水氢氟酸,静止沉降24h,所得澄清液(含氟化钾40%左右)送至真空蒸发器进行真空浓缩(压力为79993 Pa)、待溶液中含有大部分结晶时,再经过滤(压力为0.2~0.3 Mpa)、真空干燥(压力为79993 Pa)6h,制得氟化钾成品。其反应方程式如下:
2.氢氟酸与碳酸钾反应以制取氟化钾和二水氟化钾。取50g 46%的氢氟酸,置于聚乙烯的烧杯中,加入26g水,使稀释至约30%,在搅拌下缓缓加入约79g碳酸钾(不含氯离子),使溶液呈弱酸性。将溶液通过活性炭过滤。滤液在铂皿或银制蒸发皿中蒸发除去部分水分,冷却后,KF·2H2O成糊状结晶析出。用铂漏斗吸滤,结晶放在滤纸夹层中,真空烘箱脱水(40℃)。不能使其熔融(熔点46℃)。由二水合物脱水可得无水氟化钾。
3.由氟化氢钾热分解可得最纯的氟化钾。将氟化氢钾KHF2置于铂皿中,上面盖一个铂漏斗,在通风橱里加热使之分解,通过漏斗管急速吹入干燥的氮气,以带走产生的HF,纯的氟化钾则留在铂皿中。
4.商品试剂氟化钾一般为“无水”的,但实际上含有一些水。将这种氟化钾磨成细粉,在180一210℃的烘箱中保持48小时。.将其存放于于燥器中。用前将粉状的盐再在180℃于燥3小时,在热的(50℃)玻璃研钵中再次磨细。
用途
1.用于玻璃雕刻、食物防腐、电镀。可用作焊接助熔剂、杀虫剂、有机化合物的氟化剂、催化剂、吸收剂(吸收HF和水分)等。也是制取氟化氢钾的原料。
2.用作分析试剂、络合物形成剂,及用于玻璃雕刻和食物防腐,还用作杀虫剂、氟化剂等。[18]
安全信息
危险运输编码:UN 1812 6.1/PG 3
危险品标志: 有毒
有毒
危险标识:R23/24/25
文献
1. Kim, D. W.; Song, C. E.; Chi, D. Y. J. Am. Chem. Soc., 2002, 124, 10278. 2. Kotun, S. P.; Anderson, J. D. O.; DesMarteau, D. D. J. Org. Chem., 1992, 57, 1124. 3. Rergers, S. H.; Noheda, P.; Whelan, J.; Bosnich, B. J. Am. Chem. Soc., 1992, 114, 2121. 4. Hatanaka, Y.; Fukushima, S.; Hiyama, T. Tetrahedron, 1992, 48, 2113. 5. Emsley, J.; Hoyte, O. P. A.; Overill, R. E. J. Am. Chem. Soc., 1978, 100, 3303. 6. Barluenga, J.; Andina, F.; Fernández-Rodrıíguez, M. A.; García-García, P.; Merino, I.; Aguilar, E. J. Org. Chem., 2004, 69, 7352. [1~6]参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7 [7~18]参考书:危险beplay体育首页 安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
备注
暂无





 沪公网安备 31010602001115号
沪公网安备 31010602001115号