| 物竞编号 | 0CAD |
|---|---|
| 分子式 | C10H14NiO4 |
| 分子量 | 256.91 |
| 标签 | 2,4-戊二酮二水镍, 2,4-Pentanedione nickel(II) derivative, Ni(acac)2, 催化剂 |
编号系统
CAS号:3264-82-2
MDL号:MFCD00000024
EINECS号:221-875-7
RTECS号:SA2100000
BRN号:4157970
PubChem号:24857123
物性数据
1. 性状:亮绿色晶体或粉末,固态时以三聚体存在。易潮解。
2. 密度(g/mL,25/4℃):不确定
3. 相对蒸汽密度(g/mL,空气=1):不确定
4. 熔点(ºC):238
5. 沸点(ºC,常压):不确定
6. 沸点(ºC,24mm):不确定
7. 折射率:不确定
8. 闪点fp(ºC):不确定
9. 比旋光度(º):不确定
10. 自燃点或引燃温度(ºC):不确定
11. 蒸气压(kPa,25ºC):不确定
12. 饱和蒸气压(kPa,60ºC):不确定
13. 燃烧热(KJ/mol):不确定
14. 临界温度(ºC):不确定
15. 临界压力(KPa):不确定
16. 油水(辛醇/水)分配系数的对数值:不确定
17. 爆炸上限(%,V/V):不确定
18. 爆炸下限(%,V/V):不确定
19. 溶解性:溶于醚、芳烃和卤代烃类溶剂。
毒理学数据
1、急性毒性:小鼠腹腔LD50: 125mg/kg,毒性作用的细节没有报告以外的其他致死剂量值。
生态学数据
通常对水是不危害的,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1、 氢键供体数量:0
2、 氢键受体数量:6
3、 可旋转化学键数量:0
4、 互变异构体数量:6
5、 拓扑分子极性表面积(TPSA):68.3
6、 重原子数量:15
7、 表面电荷:0
8、 复杂度:196
9、 同位素原子数量:0
10、 确定原子立构中心数量:0
11、 不确定原子立构中心数量:0
12、 确定化学键立构中心数量:0
13、 不确定化学键立构中心数量:0
14、 共价键单元数量:3
性质与稳定性
1.常温常压下稳定,墨绿色结晶。易溶于苯、氯仿、四氯化碳。在26.6644Pa压力下,170℃升华。可与水、乙醇、氨、吡啶等形成各种加合物。
2.无水固体很稳定,但具有刺激性和吸湿性,因而应隔离空气和湿气保存。镍试剂有致癌活性,操作时要做好自我保护。
贮存方法
常温,避光,通风干燥处。
合成方法
1.通过二水合乙酰丙酮镍的脱水反应和真空升华,或和甲苯的恒沸蒸馏得到无水乙酰丙酮镍。
2.二水合乙酰丙酮镍在阿布德哈登干燥器中,在100℃下加热4h,在133.322Pa下脱水干燥。如有必要可在170~210℃,在26.6644~53.3288Pa压力下升华提纯。
3.通过氯化镍与乙酰丙酮直接反应而来。
用途
乙酰丙酮镍Ni(acac)2可用于催化低聚、氢硅化、氢化、还原、交叉偶联、氧化、共轭加成、对不饱和键的加成以及重排等诸多类型的反应[1]。
乙酰丙酮镍Ni(acac)2能够实现烯烃的低聚、偶联等反应,但它本身并不具有很强的催化活性,通常需要加入路易斯酸以及合适配体才能获得高活性的催化体系。加入的路易斯酸包括烷基铝、丁基锂和硼氢化钠等,主要用于还原Ni(II) 盐,通过β-H消除过程原位形成活性前体Ni-H键。然后发生炔烃对它的插入形成Ni-C键,继而又发生另一分子烯烃对Ni-C键的插入,最后经还原消除重新获得Ni-H键催化前体,并伴随相应的低聚产物。如丁二烯的环三聚反应 (式1)[2]。
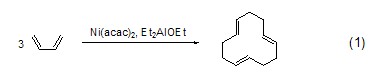
除了自身低聚反应之外,1,3-二烯化合物也能在Ni(acac)2和烷基铝试剂组成的催化体系作用下实现分子间低聚反应 (式2,式3)[3]。
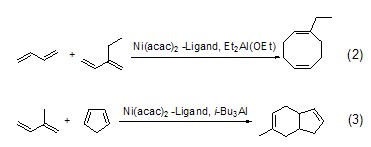
非取代和单取代炔烃也能在Ni(acac)2用下实现低聚反应,如乙炔的环四聚反应 (式4)[4]。该反应中配体的选择非常重要,弱配体如乙酰丙酮Ni(acac)2、环辛二烯cod等都有助于低聚反应的进行,而配位能力强的配体如三苯基膦则会抑止反应进行。

乙酰丙酮镍Ni(acac)2可与膦配体和还原剂如硼氢化钠组成的催化体系还能用于其它碳-碳键行成反应 (式5)[5],反应经历1,4-二烯对活化C-H键的插入反应。
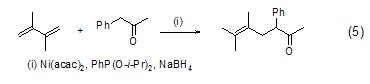
在催化剂量的乙酰丙酮镍Ni(acac)2存在下,烷基锌试剂能与α,β-不饱和酮发生共轭加成 (式6)[6]。同样的,在还原剂二异丁基氢化铝DIBAL存在下,炔基铝试剂也能与α,β-不饱和酮发生共轭加成反应 (式7)[7]。
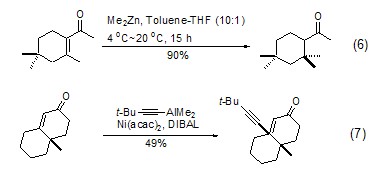
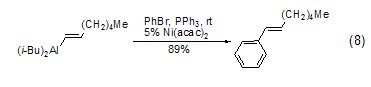
Ni(acac)2还可用于催化交叉偶联反应,加入膦配体如三苯基膦能够进一步促进该类反应 (式8)[8]。
安全信息
危险运输编码:暂无
危险品标志: 有毒
有毒
安全标识:S45 S53 S36/S37/S39
文献
1. (a) Jolly, P. W.; Wilke, G. In The Organic, Chemistry of Nickel; Academic: New York, 1975; Vols. 1 and 2. (b) Jolly, P. W. In Comprehensive Organometallic Chemistry; Wilkinson, G.; Ed.; Pergamon: New York, 1982; Vols. 7 and 8. 2. Bogdanovic, B.; Henc, B.; Karmann, H.-G.; Nussel, H.-G.; Walter, D.; Wilke, G. Ind. Eng. Chem., 1970, 62, 34. 3. Seidov, N. M.; Geidarov, M. A. Dokl. Naouk. Azerb. SSr., 1972, 28, 33. 4. Fahey, D. R. J. Org. Chem., 1972, 37, 4471. 5. Yamago, S.; Nakamura, E. Tetrahedron, 1989, 45, 3081. 6. Petrier, C.; De Souza Barbosa, J. C.; Dupuy, C.; Luche, J. -L. J. Org. Chem., 1985, 50, 5761. 7. Dayrit, F. M.; Schwartz, J. J. Am. Chem. Soc., 1980, 102, 1333. 8. Negishi, E.; Takahashi, T.; Baba, S.; Van Horn, D. E.; Okukado, N. J. Am. Chem. Soc., 1987, 109, 2393. 9.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无





 沪公网安备 31010602001115号
沪公网安备 31010602001115号