| 物竞编号 | 0C9L |
|---|---|
| 分子式 | C10H11IO4 |
| 分子量 | 322.10 |
| 标签 | 醋酸碘苯, 碘苯二乙酯, 亚碘酰苯乙酸酯, 二乙酰基碘苯, DIB, Iodobenzene Diacetate, 温和氧化剂 |
编号系统
CAS号:3240-34-4
MDL号:MFCD00008692
EINECS号:221-808-1
RTECS号:DA3525000
BRN号:1879369
PubChem号:24858980
物性数据
1. 性状:白色固体
2. 密度(g/mL,25/4℃):无可用
3. 相对蒸汽密度(g/mL,空气=1):无可用
4. 熔点(ºC):161-163
5. 沸点(ºC,常压):无可用
6. 沸点(ºC,5.2kPa):无可用
7. 折射率:无可用
8. 闪点(ºC):无可用
9. 比旋光度(º):无可用
10. 自燃点或引燃温度(ºC):无可用
11. 蒸气压(kPa,25ºC):无可用
12. 饱和蒸气压(kPa,60ºC):无可用
13. 燃烧热(KJ/mol):无可用
14. 临界温度(ºC):无可用
15. 临界压力(KPa):无可用
16. 油水(辛醇/水)分配系数的对数值:无可用
17. 爆炸上限(%,V/V):无可用
18. 爆炸下限(%,V/V):无可用
19. 溶解性:不溶于水,能够溶于大多数有机溶剂。通常在MeOH、MeCN和AcOH溶剂中使用
毒理学数据
暂无
生态学数据
该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
1、摩尔折射率:无可用
2、 摩尔体积(cm3/mol):无可用
3、 等张比容(90.2K):无可用
4、 表面张力(dyne/cm):无可用
5、 极化率:无可用
计算化学数据
1.疏水参数计算参考值(XlogP):2.8
2.氢键供体数量:0
3.氢键受体数量:4
4.可旋转化学键数量:5
5.互变异构体数量:无
6.拓扑分子极性表面积52.6
7.重原子数量:15
8.表面电荷:0
9.复杂度:220
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.遵照规定使用和储存则不会分解。
2.对空气和湿气比较稳定。
贮存方法
在干燥阴凉处储藏。
合成方法
1.通过碘苯在乙酸中被过氧乙酸氧化来制备[1]。
2.注意!要避免吸入过氧酸蒸气或皮肤接触其液体。此反应应在通风橱中进行。
在200毫升烧杯中放磁力搅拌子,其中盛20 .4克(0.10摩尔)碘苯,将烧杯浸在30℃的水浴中,在良好搅拌下,在30一40分钟内滴加36克(31毫升,0.24摩尔)工业品40%过乙酸。继续在30℃浴温搅拌20分钟,即生成均相的黄色溶液。此时,二乙酸亚碘酰苯可能开始结晶。 将烧杯浸在冰浴中1小时,在布氏漏斗上过滤,收集二乙酸盐晶体,用三份20毫升冷水洗搽。在漏斗上吸滤30分钟后,将二乙酸盐放在有氧化钙的真空干燥器中过液。得于燥的二乙酸亚碘酸苯26.7-29.3克(83一91%)。其纯度为97-98%适合大多数用途。在5M乙酸中重结晶其纯度可提高到99一100%。
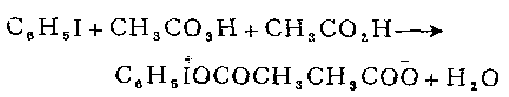
用途
(二乙酰氧基碘)苯 (DIB) 是一个在有机合成中应用非常广泛的温和型选择性氧化试剂。它有许多功能非常类似于铅试剂和铊试剂,但是具有较小的毒性和较好的反应结果。对于它的性质和应用已经有文献进行了比较详细的综述[2],这里仅对几个成熟且得到广泛应用的性质进行举例。
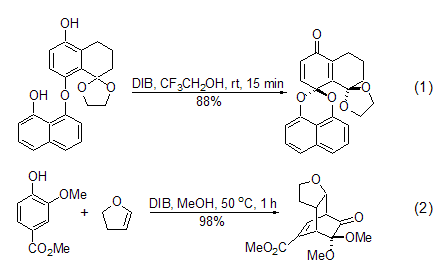
DIB 可以氧化酚产生自由基,使酚的芳香结构被破坏生成苯醌,同时在邻位或者对位发生取代反应[3]。分子内的取代反应具有重要的合成价值,可以用于天然产物的合成 (式1)[4,5]。如果有亲二烯体存在的话,生成的苯醌还可以随即发生Diels-Alder反应 (式2)[6]。
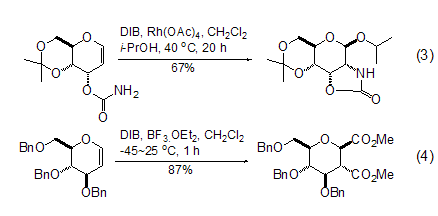
在DIB存在下可以使烯烃发生加成反应,加成到烯烃上的官能团可以完全来自DIB之外[7],也可以部分[8]或者完全来自于DIB[9]。该反应在糖的烯醇醚加成反应上具有更重要的合成价值 (式3,式4)。
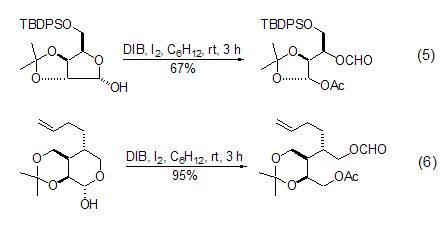
DIB与半缩醛反应发生C-C键的断裂是该试剂传统而不断更新的一个重要反应。选择稠环半缩醛底物可以获得非常有价值的扩环产物,常常用于合成九元环或者十元环的目标产物[10]。糖化学中有大量的半缩醛底物,它们与DIB反应可以获得一般方法难以得到的糖衍生物 (式5,式6)[11,12]。
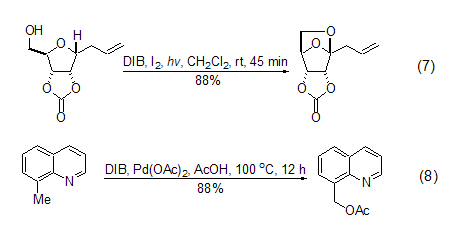
最近文献中报道DIB可以将底物中与氧原子相连的碳原子上的C-H键活化(式7)[13]。更有意义的是,金属Pd可以催化氮原子γ-碳原子上C-H键的活化,这种选择性主要是因为金属Pd首先与氮原子和γ-碳原子生成了具有五元环结构的配合物 (式8)[14,15]。
安全信息
危险运输编码:UN 1479
危险品标志: 刺激
刺激
危险标识:R36/37/38
文献
1. Sharefkin, J. G.; Saltzman, H. Org. Synth., 1973, Coll. Vol. V, 660. 2. 综述文献见:(a) Kitamura, T.; Fujiwara, Y. Org. Prep. Proced. Int., 1997, 29, 409. (b) Wirth, T. Angew. Chem. Int. Ed., 2005, 44, 3656. 3. Churcher, I.; Hallett, D.; Magnus, P. J. Am. Chem. Soc., 1998, 120, 3518. 4. Wipf, P.; Jung, J.-K. J. Org. Chem., 2000, 65, 6319. 5. Canesi, S.; Bouchu, D.; Ciufolini, M. A. Org. Lett., 2005, 7, 175. 6. Gao, S.-Y.; Ko, S.; Lin, Y.-L.; Peddinti, R. K.; Liao, C.-C. Tetrahedron, 2001, 57, 297. 7. Kirschning, A.; Hashem, Md. A.; Monenschein, H.; Rose, L.; Schoning, K.-U. J. Org. Chem., 1999, 64, 6522. 8. Levites-Agababa, E.; Menhaji, E.; Perlson, L. N.; Rojas, C. M. Org. Lett., 2002, 4, 863. 9. Shi, L.; Kim, Y.-J.; Gin, D. Y. J. Am. Chem. Soc., 2001, 123, 6939. 10. Kaino, M.; Naruse, Y.; Ishihara, K.; Yamamoto, H. J. Org. Chem., 1990, 55, 5814. 11. Khan, N.; Cheng, X.; Mootoo, D. R. J. Am. Chem. Soc., 1999, 121, 4918. 12. Cheng, X.; Khan, N.; Kumaran, G.; Mootoo, D. R. Org. Lett., 2001, 3, 1323. 13. Francisco, C. G.; Herrera, A. J.; Suarez, E. J. Org. Chem., 2002, 67, 7439. 14. Dick, A. R.; Hull, K. L.; Sanford, M. S. J. Am. Chem. Soc., 2004, 126, 2300. 15. Desai, L. V.; Hull, K. L.; Sanford, M. S. J. Am. Chem. Soc., 2004, 126, 9542. 16.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无








 沪公网安备 31010602001115号
沪公网安备 31010602001115号