| 物竞编号 | 0JYC |
|---|---|
| 分子式 | C4H9NSi |
| 分子量 | 81.15 |
| 标签 | 三甲基氰硅烷, 三甲基硅烷基氰, 三甲基硅化腈, 氰基三甲基硅烷, 三甲基硅烷基氰化物, 三甲基硅氰, 氰化三甲基硅烷, Trimethyl-silanecarbonitril, Trimethylsilycyanide, TMSCN, Trimethylsilanecarbonitrile, Trimethylsilyl cyanide, Trimethyilnitrile, Trimethylsilyl cyanosilane, Cyanotrimethylsilane, 硅烷试剂 |
编号系统
CAS号:7677-24-9
MDL号:MFCD00001765
EINECS号:231-657-3
RTECS号:暂无
BRN号:1737612
PubChem号:24889714
物性数据
1. 性状:无色杏仁状液体,剧毒、可燃性液体。
2. 密度(g/mL 25ºC):0.74
3. 相对蒸汽密度(g/mL,空气=1):未确定
4. 熔点(ºC):11~12
5. 沸点(ºC,常压):118~119
6. 沸点(ºC,5.2kPa):未确定
7. 折射率(n20/D):1.3920
8. 闪点(ºC,):未确定
9. 比旋光度(º):-未确定
10. 自燃点或引燃温度(ºC):未确定
11. 蒸气压(kPa,25ºC):未确定
12. 饱和蒸气压(kPa,60ºC):未确定
13. 燃烧热(KJ/mol):未确定
14. 临界温度(ºC):未确定
15. 临界压力(KPa):未确定
16. 油水(辛醇/水)分配系数的对数值(25℃):未确定
17. 爆炸上限(%,V/V):未确定
18. 爆炸下限(%,V/V):未确定
19. 溶解性(mg/mL):溶于大多数有机溶剂,如二氯甲烷、氯仿等,与水等质子性溶剂剧烈反应。
毒理学数据
暂无
生态学数据
对水是危害的,若无政府许可,勿将材料排入周围环境。
分子结构数据
暂无
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:1
4.可旋转化学键数量:0
5.互变异构体数量:无
6.拓扑分子极性表面积23.8
7.重原子数量:6
8.表面电荷:0
9.复杂度:81.5
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.如果遵照规格使用和储存则不会分解。
2.避免接触氧化物,酸,水分/潮湿。
3.对湿气敏感,为易燃性液体,应保存在惰性气体中。另外,该试剂为剧毒性物质,与水等反应生成氢氰酸。
贮存方法
保存在惰性气体中。
合成方法
在1升烧瓶中盛65克(1摩尔)干燥氛化钾,43.4克和0.4摩尔)三甲基氯硅烷和1}}毫升N一甲基吡咯烷酮。在机械搅拌下加热过夜(16小时)。此时回流温度达到大约105℃。接上蒸馏头和长15厘米的分馏柱,在蒸出少量含六甲基二硅氧烷和氛基三甲基硅烷的混合物前彼分后,收集纯产物,得28.0克(71%)。
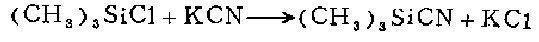
用途
1. 羰基化合物、环氧化合物、酰氯、苯醌等的氰硅烷化试剂。由醛合成酮。与Schiff碱、肟生成氨基腈。
2.三甲基氰基硅烷是一种有效的硅烷化试剂,常用于醛和酮的硅氰基化。
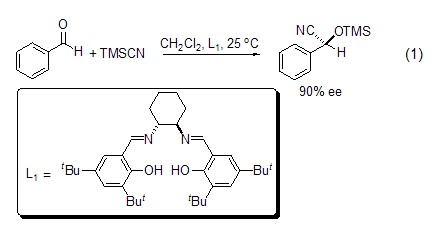
三甲基氰基硅醚及其衍生物的合成 在三甲基氰基硅烷和路易斯酸的作用下,醛和酮能够迅速转化为相应的氰基化硅醚化合物。在手性催化剂存在下,羰基化合物与TMSCN反应,产物具有很高的非对映体选择性[1,2],如三甲基氰基硅烷对醛的不对称加成 (式1)[1]。
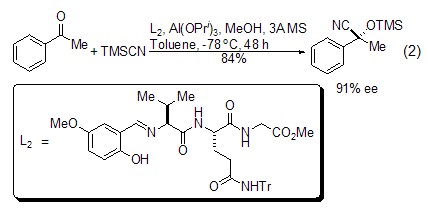
式2为三甲基氰基硅烷对酮的不对称加成[3~6]。
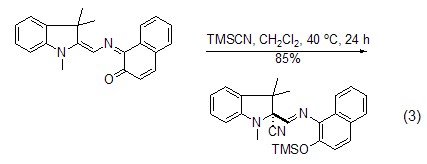
共轭加成反应 在路易斯酸的存在下,不饱和羰基化合物与TMSCN作用,发生共轭加成得到相应的加成产物 (式3)[7]。
与其它不饱和双键的加成 在适当的条件下,TMSCN能够与碳-碳双键、碳-氮双键等直接加成得到氰化物[8~11]。以THF作溶剂,在CsF存在下,TMSCN与碳-氮双键直接加成,该反应具有很高的非对映选择性 (de > 98%) (式4)[8]。

与环氧化合物、氧杂环以及氮杂环化合物的开环加成反应 在路易斯酸的作用下,环氧化合物[12]和氮杂环化合物[13]等能够与TMSCN发生开环加成反应。如环氧化物与TMSCN发生开环加成,产物为O-端保护的硅醚化合物 (式5)。

氮杂环化合物与TMSCN发生开环加成,产物为N-端保护的硅醚化合物,在酸的作用下脱TMS后得到胺类化合物 (式6)[13]。
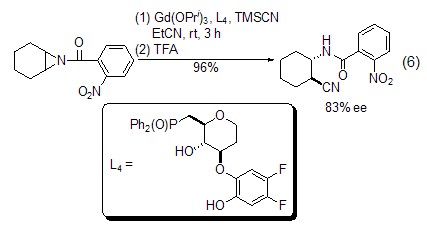
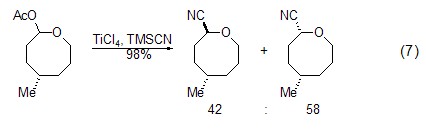
取代反应 在路易斯酸的存在下,三甲基氰基硅烷可与酯基等发生取代反应,生成相应的氰化物 (式7)[14]。
安全信息
危险运输编码:UN3384 6.1/PG 1
危险品标志: 极毒
极毒  危害环境
危害环境
安全标识:S16 S45 S36/S37/S39
文献
1. Belokon, Y. N.; North, M.; Maleev, V. I.; Voskoboev, N. V.; Moskalenko, M. A.; Peregudov, A. S.; Dmitriev, A. V.; Ikonnikov, N. S.; Kagan, H. B. Angew. Chem., Int. Ed., 2004, 43, 4085. 2. Qin, Y.-C.; Liu, L.; Pu, L. Org. Lett., 2005, 7, 2381. 3. Deng, H.; Isler, M. P.; Snapper, M. L.; Hoveyda, A. H. Angew. Chem., Int. Ed., 2002, 41, 1009. 4. Chen, F.-X.; Zhou, H.; Liu, X.; Qin, B.; Feng, X.; Zhang, G.; Jiang, Y. Z. Chem. Eur. J., 2004, 10, 4790. 5. Wilkinson, H. S.; Grover, P. T.; Vandenbossche, C. P.; Bakale, R. P.; Bhongle, N. N.; Wald, S. A.; Senanayake, C. H. Org. Lett., 2001, 3, 553. 6. Chen, F.; Feng, X.; Qin, B.; Zhang, G.; Jiang, Y. Org. Lett., 2003, 5, 949. 7. Malatesta, V.; Neri, C.; Wis, M. L.; Montanari, L.; Millini, R. J. Am. Chem. Soc., 1997, 119, 3451. 8. Li, B.-F.; Yuan, K.; Zhang, M.-J.; Wu, H.; Dai, L.-X.; Wang, Q. R.; Hou, X.-L. J. Org. Chem., 2003, 68, 6264. 9. Takamura, M.; Hamashima, Y.; Usuda, H.; Kanai, M.; Shibasakai, M. Angew. Chem., Int. Ed., 2000, 39, 1650. 10. Solé, D.; Cancho, Y.; Llebaria, A.; Moretó, J. M.; Delgado, A. J. Org. Chem., 1996, 61, 5895. 11. Krueger, C. A.; Kuntz, K. W.; Dzierba, C. D.; Wirschun, W. G.; Gleason, J. D.; Snapper, M. L.; Hoveyda, A. H. J. Am. Chem. Soc., 1999, 121, 4284. 12. Schaus, S. E.; Jacobsen, E. N. Org. Lett., 2000, 2, 1001. 13. Mita, T.; Fujimori, I.; Wada, R.; Wen, J.; Kanai, M.; Shibasaki, M. J. Am. Chem. Soc., 2005, 127, 11252. 14. Chamberland, S.; Woerpel, K. A. Org. Lett., 2004, 6, 4739 15.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无

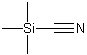





 沪公网安备 31010602001115号
沪公网安备 31010602001115号