| 物竞编号 | 0BJ1 |
|---|---|
| 分子式 | C8H11N |
| 分子量 | 121.18 |
| 标签 | (S)-苯乙胺, (S)-α-甲基苄基胺, S(-)-1-苯基乙胺, (S)-(-)-1-苯乙胺, (S)-(-)-1-Phenylethylamine, (S)-(-)-alpha-Methylbenzylamine, 光学分割剂 |
编号系统
CAS号:2627-86-3
MDL号:MFCD00064406
EINECS号:220-098-0
RTECS号:DP5775000
BRN号:2204907
PubChem号:24887137
物性数据
1. 性状:无色至浅黄色液体
2. 密度(g/mL,25/4℃):0.95
3. 相对蒸汽密度(g/mL,空气=1):无可用
4. 熔点(ºC):无可用
5. 沸点(ºC,常压):187
6. 沸点(ºC,2.9kPa):84
7. 折射率:1.526
8. 闪点(ºC):79
9. 比旋光度(º):-40(C=neat)
10. 自燃点或引燃温度(ºC):无可用
11. 蒸气压(kPa,25ºC):无可用
12. 饱和蒸气压(kPa,60ºC):无可用
13. 燃烧热(KJ/mol):无可用
14. 临界温度(ºC):无可用
15. 临界压力(KPa):无可用
16. 油水(辛醇/水)分配系数的对数值:无可用
17. 爆炸上限(%,V/V):无可用
18. 爆炸下限(%,V/V): 无可用
19. 溶解性:微溶于水,能够溶于大多数有机溶剂。
毒理学数据
暂无
生态学数据
该物质对环境可能有危害,对水体应给予特别注意。
分子结构数据
1、 摩尔折射率:39.34
2、 摩尔体积(cm3/mol):126.6
3、 等张比容(90.2K):311.5
4、 表面张力(dyne/cm):36.5
5、 极化率(10-24cm3):15.59
计算化学数据
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:1
3.氢键受体数量:1
4.可旋转化学键数量:1
5.互变异构体数量:无
6.拓扑分子极性表面积26
7.重原子数量:9
8.表面电荷:0
9.复杂度:74.6
10.同位素原子数量:0
11.确定原子立构中心数量:1
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
性质与稳定性
1.如果遵照规格使用和储存则不会分解。
贮存方法
在氮气气氛下可长期保存。
合成方法
实验室可以通过手性酒石酸对外消旋化合物进行手性拆分。
用途
手性α-甲基苄基胺的两个对映异构体在不对称合成中具有重要的地位。一方面该化合物可以大规模地商品化,是一个手性源化合物。另一方面,它独特的苄胺结构可以方便地发生脱苄基反应。因此成为一个重要的手性辅助bepaly tw 。
手性α-甲基苄基胺最成熟的功能之一是对外消旋羧酸的手性拆分[1,2]。将该化合物与外消旋羧酸在合适的溶剂中搅拌,生成一对非对映异构体的混合物。由于两者的物理性质不同,例如:溶解度不同,许多时候其中的一个对映异构体会自动从溶剂中结晶出来。如果选用合适的溶剂进行分步结晶,有时会得到非常理想的分离效果 (式1)。

手性α-甲基苄基胺也常常用于不对称反应中对映异构体纯度的鉴定。通过与所测定的对映异构体混合物反应引入一个新的手性中心,得到一对非对映异构体。这样就可以简单地通过NMR的方法来了解不对称反应的对映体选择性能力 (式2)[3]。

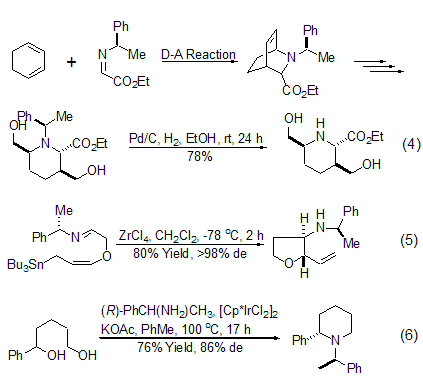
手性α-甲基苄基胺最大的用途是作为手性合成反应的辅助试剂,它利用自身的手性在反应中诱导或者控制产物的立体化学。待反应完成后,利用氢解反应脱去苄基。在这些情况下,试剂分子中的氮原子留在了产物的分子中,成为合成手性含氮化合物最惯用的策略。环氧化合物的手性开环氨基化反应是该试剂参与的一个重要反应 (式3)[4~6]。

手性α-甲基苄基胺与适当的羰基生成手性亚胺后参与的一些反应也是合成手性氮环化合物的重要方法。例如:手性亚胺与二烯进行杂原子Diels-Alder (D-A) 反应生成手性氮环化合物,然后脱去苄基得到理想的产物 (式4)[7,8]。手性亚胺也可以用于其它类型手性化合物的合成 (式5)[7~9]。但是,手性α-甲基苄基胺作为手性辅助试剂有一个致命而且不能克服的缺点,就是被诱导的产物的对映异构体纯度一般不高。原因在于该试剂结构的本质,因为在与氨基相连的手性碳原子周围缺乏合适的空间位阻 (式6)[10,11]。
安全信息
危险运输编码:UN 2922 8/PG 2
危险品标志: 刺激
刺激  腐蚀
腐蚀
安全标识:S26 S28 S45 S36/S37/S39
文献
1. Boussac, H.; Crassous, J.; Dutasta, J. P.; Grosvalet, L.; Thozet, A. Tetrahedron: Asymmetry, 2002, 13, 975. 2. Khanjin, N. A.; Hesse, M. Helv. Chim. Acta, 2003, 86, 2028. 3. Hoye, R. C.; Baigorria, A. S.; Danielson, M. E.; Pragman, A. A.; Rajapakse, H. A. J. Org. Chem., 1999, 64, 2450. 4. Sagawa, S.; Abe, H.; Hase, Y.; Inaba, T. J. Org. Chem., 1999, 64, 4962. 5. Yamauchi, Y.; Katagiri, T.; Uneyama, K. Org. Lett., 2002, 4, 173. 6. Harfouche, J.; Herault, D.; Tommasino, M. L.; Pellet-Rostaing, S.; Lemaire, M. Tetrahedron: Asymmetry, 2004, 15, 3413. 7. Maison, W.; Grohs, D. C.; Prenzel, A. H. G. P. Eur. J. Org. Chem., 2004, 1527. 8. Alonso, D. A.; Bertilsson, S. K.; Johnsson, S. Y.; Nordin, S. J. M.; Sodergren, M. J.; Andersson, P. G. J. Org. Chem., 1999, 64, 2276. 9. Park, J.-Y.; Kadota, I.; Yamamoto, Y. J. Org. Chem., 1999, 64, 4901. 10. Fujita, K.-i.; Fujii, T.; Yamaguchi, R. Org. Lett., 2004, 6, 3525. 11. Hedberg, C.; Pinho, P.; Roth, P.; Andersson, P. G. J. Org. Chem., 2000, 65, 2810. 12.参考书:现代有机bepaly tw <性质、制备和反应>;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
备注
暂无









 沪公网安备 31010602001115号
沪公网安备 31010602001115号